企鹅
65年前FDA批准用于血压控制的药物可能有助于预防癌症扩散到远处器官。最新发表于Cancer Cell杂志上的研究表明,这种药物通过保护健康细胞免受肿瘤释放的有害囊泡的影响,破坏动物模型中转移“肥沃”环境的形成。
为了使癌症扩散,癌细胞需要在远端的器官中有一个“好客”的环境。这种肥沃的“土壤”可以为循环的恶性细胞提供生存环境。最近的研究表明,来自原发肿瘤的癌细胞可以通过发送小囊泡来帮助准备这种土壤。这些囊泡含有一种分子混合物,可以“教育”健康细胞,在靶组织中为癌细胞的种子和繁殖做准备。阻断这一过程提供了一种阻止转移的策略。
宾夕法尼亚大学兽医学院的一项最新研究发现,一种FDA批准的药物与外科手术一起使用时,会妨碍动物模型中的癌症转移。该研究小组发现,在65年前开发并批准用于控制血压的药物——resperine(利血平)——还可以防止肿瘤来源的细胞外囊泡(TEV)与健康细胞融合而传递其促进疾病的分子。
“无论我们做什么来杀死癌细胞,手术或放疗或化疗,都会导致应激,数据显示应激会刺激这些囊泡的产生,”宾大的生物学家Serge Fuchs说。“因此,我们的想法是,作为该主要治疗的佐剂,谨慎地限制这些囊泡对健康组织的影响,从而防止恶性细胞的扩散。”
Resperine抑制细胞外囊泡被摄取
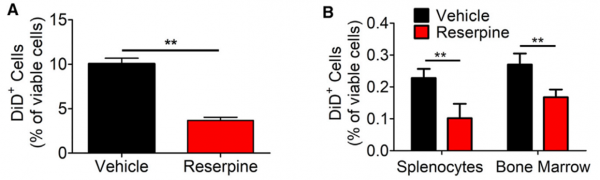
该研究的发现发表于Cancer Cell杂志,结果表明,在手术前后,给予黑色素瘤小鼠适度剂量的resperine会破坏健康细胞对TEV的摄取,减少癌症的扩散,并显著延长动物的存活时间。
虽然先前的研究表明TEV可以促进转移性疾病,并且在某些情况下可以将正常细胞转化为恶性细胞,但很明显,并非每个与这些囊泡接触的健康细胞都会发生癌变。因此,科学家们假设健康细胞可能拥有一种防御这种转变的策略。这种防御机制可能是抗转移治疗的靶标。
为了寻找推测的防御机制,Fuchs及其同事将人类细胞暴露于黑色素瘤细胞的TEV后,观察人类细胞上哪些表面蛋白质的数量发生了变化。其中一个更重要的改变是IFNAR1,它是组成I型干扰素受体的蛋白质之一,Fuchs之前曾研究过这种受体。干扰素被用作癌症疗法,包括对抗恶性黑素瘤,并且已知其在预防癌症扩散中起作用。
在使用体外培养的人细胞实验中,来自黑素瘤患者的囊泡处理降低了IFNAR1水平。从临床数据来看,研究人员发现患有转移性疾病的人黑色素瘤患者更可能具有较低水平的IFNAR1。
为了理解TEV如何影响健康细胞的重编程以促成转移性土壤,他们使用具有抗降解的IFNAR1的小鼠模型。他们发现,这些小鼠抵抗摄取TEV,并且没有发生黑色素瘤肿瘤的肺转移。从一系列偶然的实验线索中,研究小组发现来自这些小鼠的健康细胞不太可能摄取TEV,因为囊泡的脂质膜不能有效地融合细胞的脂质膜。
“那时,我们开始认为健康细胞持续吞噬囊泡对正常细胞的'教育'非常重要,”Fuchs说。“这向我们表明,任何会阻碍正常细胞持续吸收囊泡的事件都可能会破坏它们的重编程,并且可能是抗转移的。”
研究人员发现用25-羟基胆固醇(25HC)预处理细胞可成功抑制囊泡摄取,25-羟基胆固醇是一种由干扰素诱导的化合物,已被证明可以破坏脂质膜的融合。暴露于25HC的细胞摄取较少的TEV。进一步的实验表明,包含25HC和干扰素的途径在阻止TEV重编程正常细胞中起作用。
由于25HC在体内迅速降解,使其难以成为抗癌药物,科学家继续寻找,寻找FDA已经批准用于人类的化合物,同样会破坏TEV的摄取。他们筛查到了resperine,该药在更好的竞品出现之前一直被用于治疗高血压。
“Resperine会引起嗜睡,有时甚至会出现抑郁症,”Fuchs说。“如果你每天使用它作为降压药物,这些副作用是一个真正的麻烦,但如果我患有转移性黑色素瘤,我肯定会愿意在手术时间内忍受这些影响。”
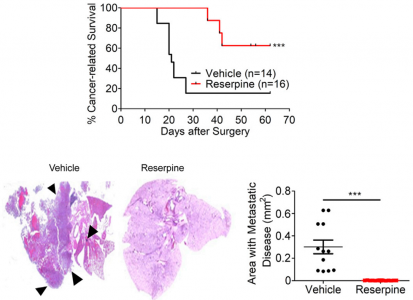
在患有黑素瘤肿瘤的小鼠中测试resperine,研究人员在去除原发肿瘤手术前后给药。虽然单独给予resperine似乎对肿瘤生长和存活几乎没有影响,但在手术前后接受resperine治疗的小鼠似乎破坏了健康细胞的重编程。研究人员报告说,这些动物的总体存活率显著提高,并且治疗“几乎消除了”肺转移的现象。
“我们迫切希望将其交到医学和兽医肿瘤学家手中,”Fuchs说。
为了跟进有希望的发现,Fuchs及其同事希望更深入地探索resperine不仅对转移,而且对囊泡形成和组成的影响。他们还希望进一步探索在健康和疾病中产生25HC的酶的作用。
利血平可显著提高黑色素瘤细胞小鼠手术后的存活率,并显著减少癌细胞转移
论文摘要:
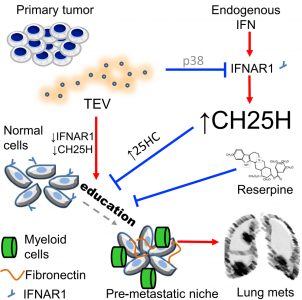
肿瘤来源的细胞外囊泡(TEV)“教育”健康细胞以促进转移。该研究发现黑色素瘤TEV下调I型干扰素(IFN)受体和IFN诱导型胆固醇25-羟化酶(CH25H)的表达。CH25H产生25-羟基胆固醇,其抑制TEV摄取。来自黑素瘤患者的白细胞中CH25H水平低与预后不良相关。不能下调IFN受体和Ch25h的小鼠对TEV摄取、TEV诱导的转移前生态位和黑素瘤肺转移具有抗性。然而,Ch25h的敲除逆转了这些表型。一种抗高血压药物利血平抑制TEV摄取并破坏TEV诱导的转移前生态位和黑素瘤肺转移瘤的形成。这些结果表明CH25H在防御TEV对正常细胞的教育中的重要性,并且在辅助黑素瘤治疗中使用利血平将有积极作用。
模式图。黑素瘤衍生的细胞外囊泡(EV)在正常细胞中下调I型干扰素受体(IFNAR1)和胆固醇25-羟化酶(CH25H),以促进EV摄取和转移前的生态位形成。 IFNAR1-CH25H上调或利血平治疗抑制EV摄取和癌细胞转移。
参考文献:
Ortiz A, Gui J, Zahedi F, Yu P, Cho C, Bhattacharya S, Carbone CJ, Yu Q, Katlinski KV, Katlinskaya YV, Handa S, Haas V, Volk SW, Brice AK, Wals K, Matheson NJ, Antrobus R, Ludwig S, Whiteside TL, Sander C, Tarhini AA, Kirkwood JM, Lehner PJ, Guo W, Rui H, Minn AJ, Koumenis C, Diehl JA, Fuchs SY. An Interferon-Driven Oxysterol-Based Defense against Tumor-Derived Extracellular Vesicles. Cancer Cell. 2019 Jan 14;35(1):33-45.e6. doi: 10.1016/j.ccell.2018.12.001. 影响因子:22.844