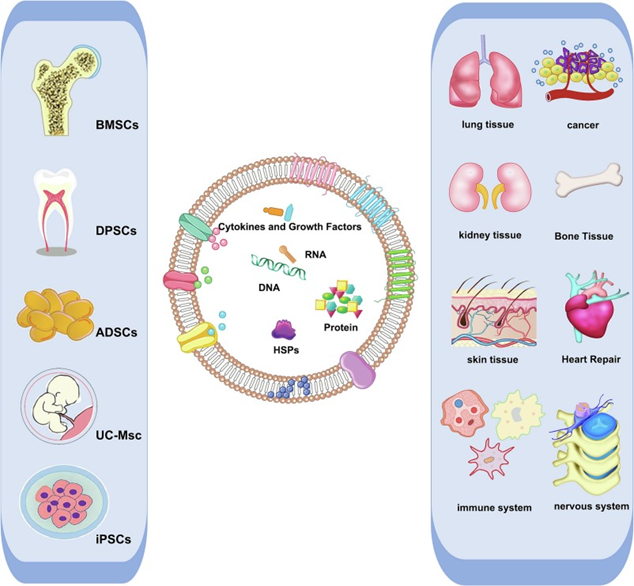
近年来,外泌体在皮肤疾病治疗领域的研究受到广泛关注,尤其是源自干细胞的外泌体(stem cell-derived exosomes,SC-Exos),由于其良好的免疫调节与组织修复能力,展现出广阔的应用前景。
近期,杭州医学院宁波市口腔医院吴训伟研究团队在国际权威期刊International Journal of Biological Macromolecules 上发表了题为“Biomaterial-enhanced delivery of stem cell-derived exosomes for skin inflammatory diseases: Mechanisms and therapeutic advances”的综述文章,系统总结了SC-Exos在皮肤炎症性疾病中的机制研究与治疗应用,并重点探讨了生物材料在其精准递送中的关键作用。

该综述指出,常见皮肤炎症性疾病如银屑病、特应性皮炎、白癜风、红斑狼疮等,通常伴随慢性免疫失调和皮肤屏障功能受损,传统治疗手段(如糖皮质激素、免疫抑制剂等)虽可缓解症状,但易复发且存在长期副作用。而SC-Exos因具有携带miRNA、蛋白质、脂类等活性物质的能力,能够有效调控T细胞、巨噬细胞、树突状细胞等免疫细胞功能,在控制炎症、促进组织再生、维持免疫平衡等方面显示出显著疗效。
文章还对不同来源的干细胞外泌体(包括脂肪来源、骨髓来源、牙髓来源、诱导多能干细胞及脐带间充质干细胞)在各种皮肤病模型中的表现进行了详细比较。例如,脂肪干细胞外泌体(ADSC-Exos)在特应性皮炎和银屑病动物模型中能够显著减轻炎症反应、增强皮肤屏障;牙髓干细胞外泌体(DPSC-Exos)在调控Treg/Th17平衡方面表现出更强的免疫调节能力;而人脐带间充质干细胞外泌体(hUCMSC-Exos)因产量高、生物活性强,在动物实验和初步临床研究中均取得良好疗效。
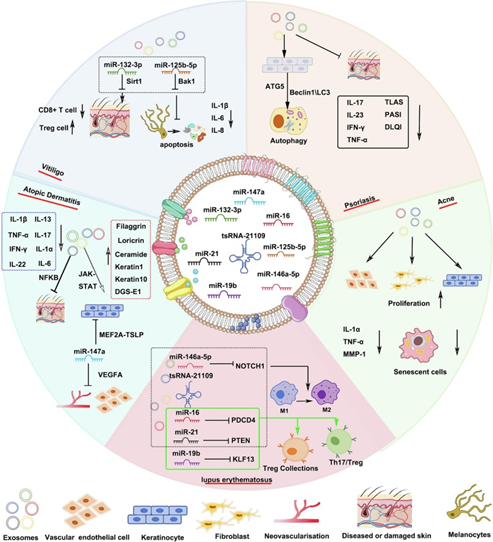
针对当前外泌体治疗面临的递送效率低、靶向性差、体内半衰期短等问题,该综述特别强调生物材料在增强外泌体递送方面的重要性。通过将外泌体负载于水凝胶、纳米颗粒或组织工程支架中,可实现其在病灶区域的缓释、靶向富集和稳定性提升。例如,壳聚糖、透明质酸、明胶等天然高分子材料不仅具备良好生物相容性,还可促进外泌体在伤口、瘢痕及炎症组织中的长期滞留和作用。纳米脂质体与金纳米颗粒等新型载体则提高了跨屏障递送与成像追踪能力。与此同时,微流控芯片和基因工程手段的发展亦为外泌体的大规模纯化与功能改造提供了新技术平台。
值得关注的是,综述中也总结了多个正在进行的外泌体临床研究,涵盖特应性皮炎、银屑病、痤疮瘢痕等疾病的治疗尝试,表明SC-Exos联合生物材料构建的新一代“智能递送系统”正逐步从实验室走向临床。
该项工作不仅为外泌体在皮肤炎症性疾病治疗中的应用提供了理论基础和机制框架,也为生物材料辅助递送系统的优化设计提供了思路。未来,随着制备技术、递送系统和临床研究的持续推进,SC-Exos有望成为皮肤疾病精准治疗的重要工具。
文章由王爽爽、庄德轩、徐啟、侯东宇、冯腾飞、郭泾、吴训伟等人共同完成,其中吴训伟研究员为通讯作者。全文已于2025年6月16日在线发表,文章链接如下:
https://doi.org/10.1016/j.ijbiomac.2025.145213
外泌体资讯网 Int J Biol Macromol| 吴训伟团队综述:干细胞外泌体结合生物材料治疗皮肤炎症性疾病的研究新进展