树突状细胞(DC)被认为是最有效的抗原呈递细胞,在介导先天免疫应答和诱导适应性免疫应答方面至关重要。DC疫苗的成功依赖于DC迁移到淋巴结和脾脏等二级淋巴组织的能力,在那里DC与T细胞相互作用,刺激并激活T细胞以促进抗肿瘤免疫。然而,注射激活的DC到体内的效果有限,因为只有少量DC短暂迁移到淋巴结,极大地限制了T细胞的激活。此外,成熟DC表面高表达的PD-L1结合其自身的B7-1,阻碍了B7-1与T细胞上CD28的结合,抑制了T细胞的有效激活。因此,有必要设计一种递送策略,以促进DC持续迁移到二级淋巴组织并促进T细胞的激活,以增强DC疫苗的抗肿瘤免疫。近日,深圳湾实验室饶浪团队与武汉大学人民医院徐细明团队合作,开发了一种新型3D树突状细胞(Dendritic Cell, DC)疫苗用于肿瘤术后的免疫治疗。该成果标题为“3D-Printed Dendritic Cell Vaccines for Post-Surgery Cancer Immunotherapy”,已发表在于Advanced Functional Materials期刊。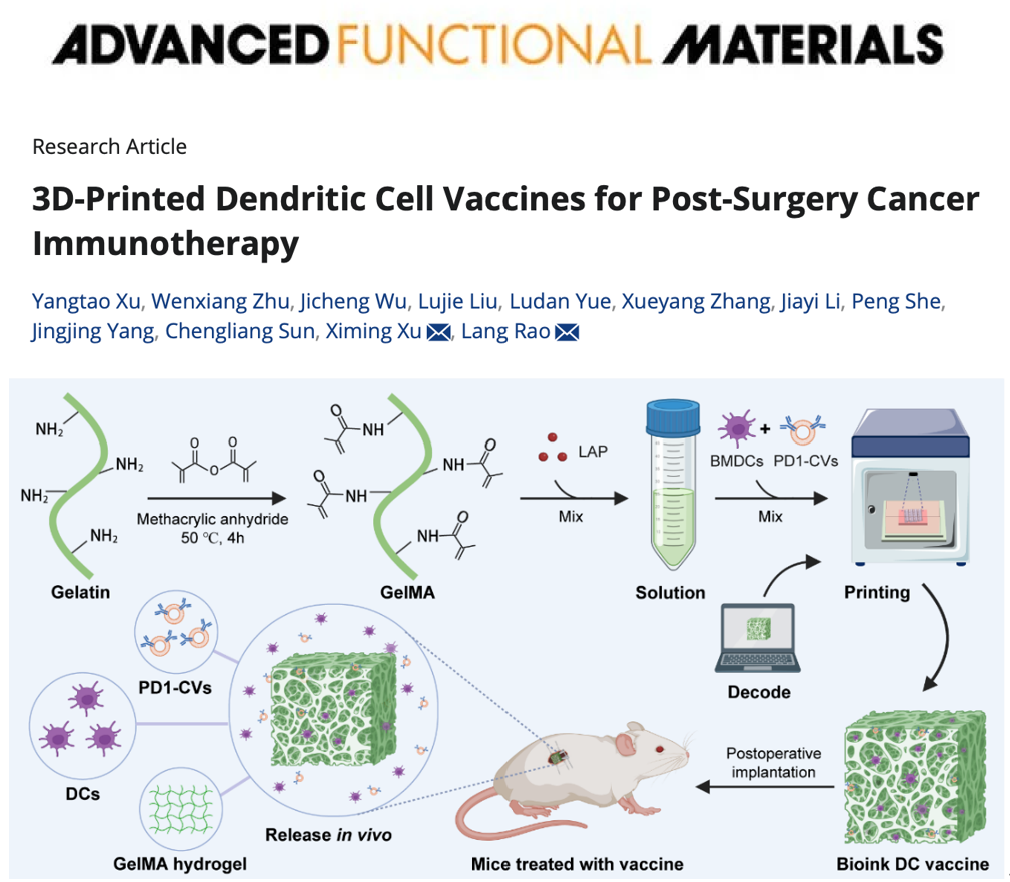
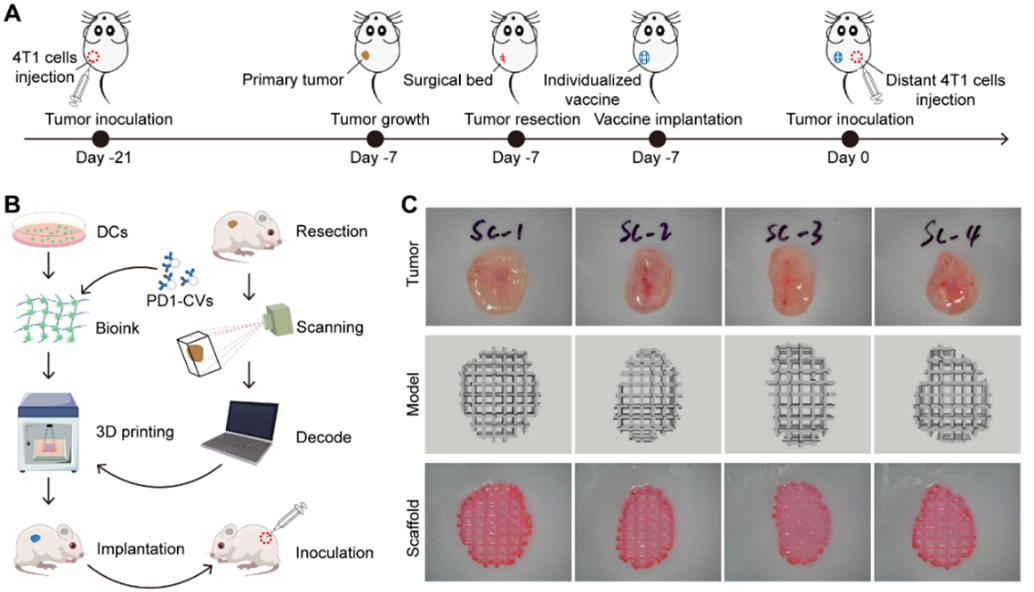
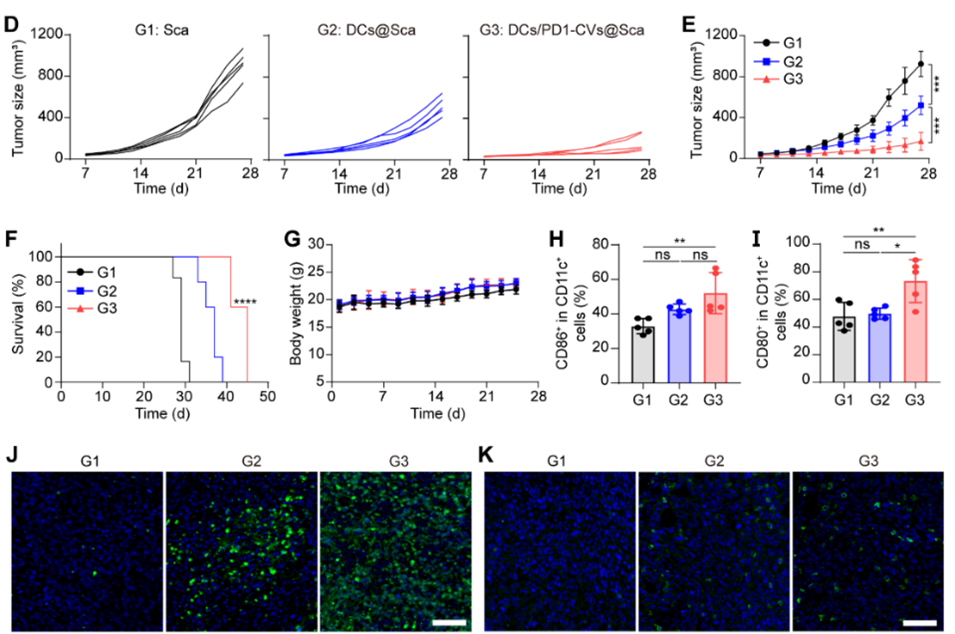
该3D打印的DC疫苗(DCs/PD1-CVs@Sca),能够显著增加DC在体内的存活时间,阻断DC表面的PD-L1,用于增强DC疫苗的抗肿瘤作用。DCs/PD1-CVs@Sca由骨髓来源的DC(BMDC)、基因编辑的高表达PD1肿瘤细胞膜囊泡(PD1-CVs)和甲基丙烯酸化水凝胶(GelMA)组成(图1)。其中GelMA为DC提供生存环境,其包裹DC打印成多孔支架将进一步提高DC的存活;PD1-CVs充当DC的免疫调节剂,刺激DC成熟的同时,阻断其表面的PD-L1,从而增强DC的抗肿瘤作用。为了验证DCs/PD1-CVs@Sca的体内抗肿瘤效果,将支架移植到小鼠皮下,7天后在小鼠对侧接种肿瘤。实验结果表明,DCs/PD1-CVs@Sca可以显著抑制肿瘤的进展。此外,DCs/PD1-CVs@Sca可以促进肿瘤中记忆CD8+ T细胞浸润,证明DCs/PD1-CVs@Sca具有长期抗肿瘤效果。同时,DCs/PD1-CVs@Sca可以促进淋巴细胞和脾脏中DC的成熟和CD8+ T细胞浸润,表明DCs/PD1-CVs@Sca促进全身的抗肿瘤作用。最后,研究团队个性化3D打印DC疫苗,用于填充肿瘤术后缺损(图2)。实验结果表明,填充后的DCs/PD1-CVs@Sca可以促进肿瘤组织的凋亡,抑制肿瘤的生长,延长了术后小鼠的生存时间(图3)。综上所述,基于3D打印,研究团队开发了一种个性化DC疫苗,用于肿瘤切除术后部位填充,抑制了远端肿瘤复发并延长了小鼠手术后的生存时间,为肿瘤术后免疫治疗提供了一种简单、安全、有效的策略。武汉大学人民医院/深圳湾实验室联培博士生徐阳涛为论文第一作者,深圳湾实验室饶浪研究员与武汉大学人民医院徐细明教授为该论文共同通讯作者。该研究得到了国家自然科学基金、广东省自然科学基金、深圳市医学科学专项基金、深圳湾实验室概念验证基金、武汉大学人民医院交叉学科创新人才项目基金等项目支持。3D-Printed Dendritic Cell Vaccines for Post-Surgery Cancer Immunotherapy链接地址:https://onlinelibrary.wiley.com/doi/full/10.1002/adfm.202400507外泌体资讯网 Adv. Funct. Mater∣深圳湾实验室饶浪/武汉大学人民医院徐细明:3D打印DC细胞囊泡疫苗用于肿瘤术后免疫治疗