CircRNA是调节肿瘤增殖和进展的非编码RNA新成员,然而结直肠癌衍生的外泌体circRNA的功能和调控机制仍不清楚。近日,来自同济大学附属同济医院李冬、孙祖俊、周永新课题组的研究人员在Molecular Cancer杂志上发表文章,揭示了结直肠癌分泌的外泌体circRNA——circPACRGL,通过充当miR-142-3p/miR-506-3p海绵增强CRC细胞的增殖。
结直肠癌(CRC)是最常见的恶性肿瘤之一,具有高转移和复发的风险。常规CRC疗法具有毒性和不耐受性等缺点,临床结果不能令人满意。因此,迫切需要敏感的CRC生物标志物以进行早期检测并探索用于CRC治疗的新靶标。外泌体在肿瘤中的功能引起了越来越多的关注。外泌体是由各种类型的细胞分泌的小脂质双层膜泡,直径约30-100nm。越来越多的证据表明,肿瘤外泌体通过转移和交换致癌分子(包括circRNA、microRNA、mRNA、蛋白质和脂质)在肿瘤细胞间的通讯中发挥关键作用,从而参与肿瘤发生、肿瘤增殖、肿瘤转移、血管生成、免疫逃逸和耐药性。
环状RNA(circRNA)已被鉴定为具有闭环结构且无5'和3'末端的非编码RNA(ncRNA)家族的成员,与包括CRC在内的肿瘤的发生和发展密切相关。此外,circRNAs在外泌体中富集,对于细胞间的通讯很重要。据报道,外泌体circRNAs在血液中稳定,有望成为用于临床检测的新型生物标志物。此外,MicroRNA(miRNA)是一类内源性22-25nt的非编码单链RNA,是转录后基因调控的关键调控因子。CircRNA可以充当有效的miRNA海绵,包含保守的miRNA靶位点,竞争性抑制miRNA来调节下游靶基因的表达。因此,外泌体circRNAs可能是一类新型的潜在生物标志物或肿瘤治疗的治疗靶标。然而,肿瘤来源的外泌体circRNA的功能和潜在机制仍未得到充分探索。
TGF-β是一种多功能细胞因子,与肿瘤的发生、发展和转移有关。TGF-β被认为是免疫功能的守护者,不仅调节多种肿瘤细胞的自主信号传导途径,而且还通过旁分泌机制调节肿瘤与宿主细胞之间的相互作用。此外,TGF-β促进肿瘤相关中性粒细胞的形成。特别地,在肿瘤微环境中,TGF-β抑制N1、促进N2中性粒细胞分化和肿瘤发展。TGF-β1属于TGF-β的亚家族成员,在TGF-β家族中比例最高(>90%),具有最强活性和最深入的研究。TGF-β1在细胞增殖、分化和凋亡中起着关键的调节作用,广泛参与各种生理和病理过程,包括炎症反应和肿瘤进展。在包括CRC在内的许多肿瘤类型中,TGF-β1经常被过度生产,其信号转导也出现失调。有趣的是,TGF-β1的上调抑制了早期的肿瘤生长,但促进了晚期肿瘤的生长,从而增强了恶性表型。
在这项研究中,研究人员在肿瘤衍生的外泌体中鉴定了一种新型的circRNA——circPACRGL,并进一步探讨了其在CRC进展中的功能和潜在机制。研究人员使用透射电子显微镜、纳米粒子跟踪分析(NTA)和Western blot对CRC细胞衍生的外泌体进行了表征。研究人员通过RNA测序和RT-qPCR鉴定外泌体刺激的CRC细胞中的circRNA。荧光原位杂交(FISH)法用于检测circPACRGL的细胞分布,使用生物信息学分析确定了circPACRGL的miRNA靶标。最后,流式细胞仪检测了N1-N2中性粒细胞的分化。
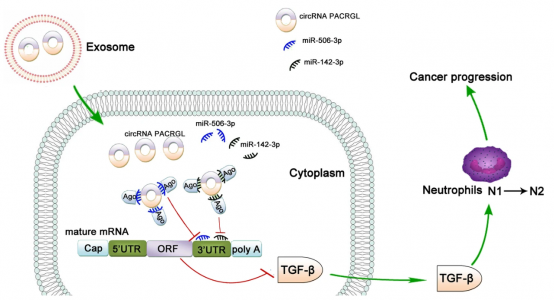
研究人员发现,添加肿瘤来源的外泌体后,circPACRGL在CRC细胞中显著上调。此外,circPACRGL充当miR-142-3p/miR-506-3p海绵,促进TGF-β1的表达。circPACRGL通过miR-142-3p /miR-506-3p-TGF-β1轴促进了CRC细胞的增殖、迁移和侵袭,以及N1向N2中性粒细胞的分化。这项研究首次揭示了肿瘤来源的外泌体circPACRGL在CRC增殖和转移中起着致癌作用,为circRNA在CRC进程中的作用提供了新机制,并且是CRC治疗的重要标志物。