土豆
目前,大多数抗癌疗法都存在着严重和有害的不良反应,减轻肿瘤治疗药物的副作用至关重要。来自四川大学高分子科学与工程学院和华西药学院张凌课题组的研究人员报告了一种基于外泌体样(ELVs)的高度生物相容性肿瘤细胞药物递送系统,将低毒性的抗癌药物西贝母碱用于非小细胞肺癌的治疗。该研究发表于Journal of Controlled Release杂志上(影响因子7.901)。
肺癌是世界范围内诊断最多的癌症类型之一,并且正在成为癌症相关死亡的主要原因之一。非小细胞肺癌(NSCLC)约占总肺癌总数的85%,在过去的几十年中,由于缺乏临床症状和有效的筛查措施,大多数NSCLC被诊断时就已处于晚期阶段,因此治疗效果很差。目前,已经开发了一些临床上较好的肺癌早期诊断方法,并且医疗条件的改善也使得早期癌症诊断正在成为现实。因此,对于早期癌症的治疗,需要开发一些新方法。而对于早期癌症的来说可能需要很长的疗程,因此需要比目前治疗方法毒性更低。新型药物和新药物递送系统对于开发此类疗法至关重要。
在该研究团队此前的工作中,已经确定将西贝母碱(imperialine)作为早期癌症治疗的良好候选药物。西贝母碱是植物川贝母(Bulbus Fritillariae cirrhosae)中的活性成分之一,是一种重要的中药抗炎药物,具有很强的抗炎症作用。研究表明,西贝母碱具有抑制NSCLC的特性,而且可能对早期肿瘤更加有效,并且可以用于高危人群的预防使用。然而,西贝母碱的半衰期短,生物分布不佳,临床应用困难。为了解决这些问题,研究人员开发了一种新型外泌体样囊泡(exosome-like vesicles,ELV)为基础的药物传递系统用于西贝母碱的给药。该ELV系统显著增强了药物在肿瘤的积累和保留,并且细胞毒性和系统毒性很低。因此,ELV系统在长期癌症治疗或癌症预防中具有极大潜力。
ELV通常被认为是40-200nm的球状细胞外囊泡(EVs),其衍生自多泡体的腔膜并从质膜或细胞表面发芽,由多种细胞类型产生,并且可以在体液中保留。由于ELV天然携带来自肿瘤细胞的某些遗传物质或蛋白质,具有强大的生物相容性和良好的负载能力,并且被认为是正常、炎症、癌细胞之间的通信媒介。在医学应用中,ELV通常被改造成为高效的药物或基因装载系统,满足更好的靶向递送能力或诊断功能。在这项研究中,研究人员广泛设计了各种ELV结构以满足需求。为了有效装载西贝母碱,研究人员开发了一种新颖的胶束辅助方法,大大改善了西贝母碱的包装。这种方法以前还从未报告过与ELV一起使用,具有极大应用潜力。研究人员设计了一种八肽cNGQGEQc(CC8)用作NSCLC的靶向配体。该配体特异性结合整合素α3β1,因为整合素α3β1在NSCLC细胞上高表达。研究人员在CC8的两个半胱氨酸残基末端添加了游离硫醇进行了修饰。此外,ELV应用的另一个挑战是从指定的细胞中收集足够的ELV。研究人员从血液中纯化了网状细胞成熟过程中释放的ELV,发现血液来源源ELV与细胞来源的ELV具有相同的效果。
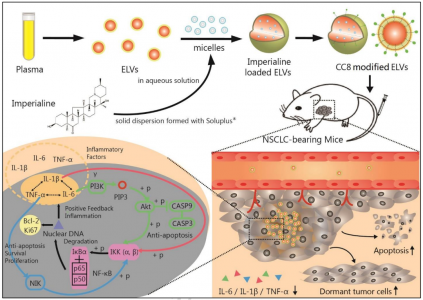
总的来说,研究人员设计并开发了一种新的ELV平台,用于递送药物并靶向NSCLC中的炎症和肿瘤细胞。从人血浆中分离ELV,并使用新颖且有效的胶束辅助包装方法将西贝母碱包封到ELV中。最后,将CC8配体连接到这些ELV上进行NSCLC细胞的靶向。体外和体内实验均表明,该ELV系统通过改善药物的肿瘤靶向性和保留度,大大提高了药物的抗肿瘤作用。该ELV系统在长期疗程中显示出巨大的潜力,因为ELV的毒性非常小并且显著提高了给药效率。研究结果提供了ELV在改善药物输送中的创新方法,为未来的研究提供了新的基础。
参考文献:Lin Q, Qu M, Zhou B, Patra HK, Sun Z, Luo Q, Yang W, Wu Y, Zhang Y, Li L, Deng L, Wang L, Gong T, He Q, Zhang L, Sun X, Zhang Z. Exosome-like nanoplatform modified with targeting ligand improves anti-cancer and anti-inflammation effects of imperialine. J Control Release. 2019; 311-312: 104-116.