外泌体用于体内递送治疗药物,包括RNAi和化学药物。然而由于它是由脂质双层膜组成,对目标细胞没有特异性识别能力,因此进入非特异性细胞可能导致潜在的副作用和毒性。体外化学修饰技术和细胞内基因工程技术已被报道用靶向配体修饰外泌体。RNA纳米颗粒已可以在外泌体表面显示肿瘤特异性配体,副作用和毒性会降低。来自美国俄亥俄州立大学的研究人员发表综述,重点介绍了RNA纳米颗粒用于外泌体表面展示化学配体、小肽或RNA适体,用于特定的癌症靶向递送治疗,介绍了靶向递送siRNA和miRNA的最新进展。相关内容以“Targeted delivery of RNAi to cancer cells using RNA-ligand displaying exosome”为题于4月19日发表在新一期的药学领域国际学术期刊Acta Pharmaceutica Sinica B杂志上。
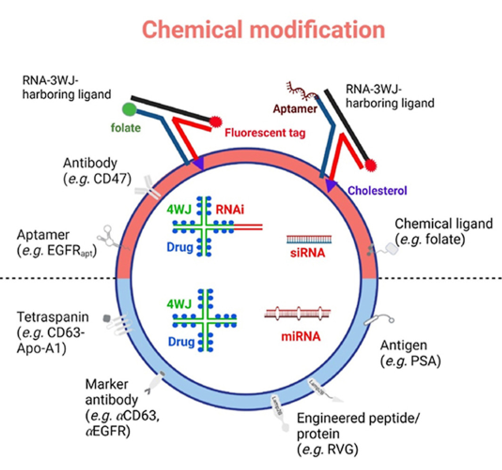
RNA干扰技术(RNAi)通过特异性基因抑制在治疗应用中具有巨大的潜力。小干扰RNA (siRNA)优于小分子和单克隆抗体,因为siRNA通过与mRNA完全的碱基配对来执行其功能。相比之下,小分子和单克隆抗体药物需要识别靶蛋白复杂的空间构象。近几十年来,siRNA疗法药物Onpattro (patisiran)首次获得了批准,用于治疗成人遗传性转甲状腺素蛋白(hATTR)淀粉样变性引起的周围神经病变。纳米技术应用于治疗学,通过减少全身毒性、克服耐药性和为联合治疗提供改进的平台,正在引领癌症治疗的新时代。然而,RNAi向癌细胞的递送策略包括阳离子脂质体、阳离子脂质体和阳离子聚合物,但特异性靶向仍然具有挑战性。此外,由于内吞作用的存在,纳米颗粒介导的递送的治疗效率经常受到不利影响。内吞作用通常导致纳米颗粒包裹,随后被溶酶体降解。外泌体最近被认为是一种优秀的治疗囊泡,通过在体内递送治疗药物,包括RNAi和化学药物,用于治疗疾病,尤其是在癌症治疗中非常有效。然而,由于外泌体没有对癌细胞的特异性识别能力,进入非特异性细胞可能导致潜在的副作用和毒性。因此,人们希望为外泌体提供一种靶向能力,将治疗药物递送到特定细胞。据报道,体外化学修饰和细胞基因工程的方法可以用靶向配体修饰外泌体。由于具有负电荷和多价性的优势,RNA纳米颗粒已被用于在外泌体表面携带肿瘤特异性配体。在大多数纳米递送系统中,内吞作用介导RNAi治疗药物(miRNA/anti-miRNA/siRNA)的细胞摄取。然而,RNAi的核内体包裹阻止了与RNA诱导沉默复合体(RISC)的相互作用及其靶向位于细胞质中的mRNA,这是RNAi治疗中最广为人知的困难之一。解决核内体诱捕的一个有吸引力的策略是向大自然学习。自然界已经进化出智能纳米机器,如外泌体作为一类细胞外囊泡(EV)。外泌体来源于晚期内体途径/多泡体(MVB)。通常,这些纳米囊泡的直径在30到150纳米之间。最近的兴趣集中在利用外泌体作为RNAi递送的纳米载体。这些纳米囊泡显示出独特的膜特性(化学成分,如脂质、肽、蛋白质等),提供了与细胞器受体膜融合的天然能力。然而,它们缺乏细胞靶向性/特异性,导致治疗效果差和潜在的毒性。采用RNA纳米技术可以增强外泌体的特异性,用于癌症治疗。在这篇综述中,研究人员讨论了RNA纳米技术的独特性质,并总结其在外泌体展示并用于特异性靶向的潜在应用。研究人员认为,RNA纳米技术具备两个优势:i)RNA纳米技术用于特异性靶向和ii)外泌体用于高效的细胞进入和核内体逃逸。研究人员展示了利用显示外泌体的RNA配体靶向药物递送到癌细胞的进展,综述了癌症治疗中的两个挑战——缺乏针对病变细胞的特异性治疗靶点和细胞进入后治疗药物的内溶酶体捕获。研究人员认为,带有细胞特异性配体的RNA纳米颗粒可能作为高效siRNA递送的强大平台,从而有可能使研究重新焕发活力。RNA纳米颗粒的多价性、阴离子性质和弹性性质使其能够快速在癌细胞积累并快速肾脏清除,这使其成为一种独特的治疗工具。在外泌体表面应用RNA纳米技术可以作为治疗癌症的极好方法。用RNAi治疗癌症的主要瓶颈之一是内溶酶体包裹。研究人员认为,RNA纳米技术的配体可以传递具有目标特异性的siRNA,并通过将货物运送到细胞质溶胶中来提高功效。他们强调,结合强大的成像技术可以评估EV相关膜融合的详细机制。总的来说,这一综述为RNA纳米技术作为将外泌体生物学转化为基于RNA的癌症治疗的基础提供了巨大的可能性。
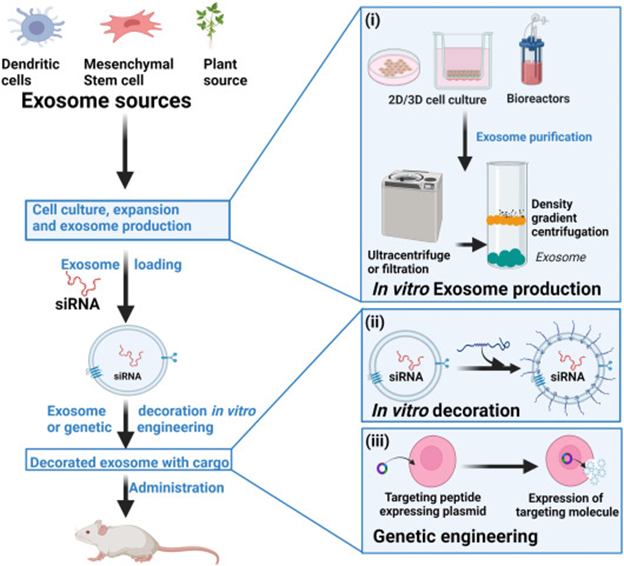
参考文献:Targeted delivery of RNAi to cancer cells using RNA-ligand displaying exosome. Acta Pharm Sin B. 2023 Apr;13(4):1383-1399.




