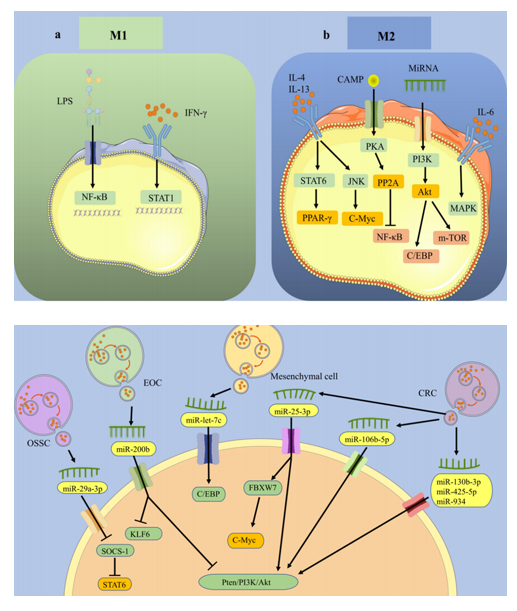
巨噬细胞(macrophage)是人体内重要的免疫细胞,在肿瘤微环境(Tumor microenvironment,TME)中起到关键作用[1]。它受到生长因子、细胞因子、微生物产物的刺激会分化成不同的表型和发挥不同的功能,称为“巨噬细胞的极化”[2]。最近的研究发现外泌体可以参与巨噬细胞和肿瘤微环境之间的信息传递,直接或者间接地影响甚至是决定巨噬细胞的极化[6],其中外泌体中携带的miRNA在近几年被认为是巨噬细胞分化、活性和极化的关键调节因子。
2022年10月5日,西南医科大学附属医院输血科王静、肿瘤科韩云炜教授团队在中科院SCI分区升级版医学一区,Top期刊Biochimica et Biophysica Acta (BBA) - Reviews on Cancer(IF: 11.414)上发表了题为“The role of exosomes in the tumour microenvironment on macrophage polarisation”的综述文章(2022 Oct 5:188811),系统介绍了肿瘤微环境的外泌体对巨噬细胞极化的影响。西南医科大学卓越医师班大四学生龙润民与王静作为文章共同作者。
该综述重点介绍了一部分M1/M2巨噬细胞在肿瘤微环境中相互转化的反应和机制,以及肿瘤微环境中的外泌体在巨噬细胞两种表型相互转化中的作用。
1.外泌体miR-934、miR-106b-5p通过PI3K/Akt途径诱导M2巨噬细胞极化
研究者在结直肠癌(Colorectal cancer,CRC)肿瘤微环境中M2巨噬细胞聚集的部位发现miR-934表达水平明显增高,并且已经证实miR-934主要来源于癌细胞衍生的外泌体。miR-934调控巨噬细胞的极化主要涉及HnRNPA2B1和Pten/PI3K/Akt途径。此外,miR-145也是由结直肠癌上皮细胞产生,通过外泌体被巨噬细胞吸收并促进巨噬细胞的替代激活[53]。
在上皮间质转化-结直肠癌体系(EMT-CRC)中,miR-106b-5p被认为是影响巨噬细胞极化的主要因素, miR-106b-5p通过抑制程序性细胞凋亡因子4(Programmed cell death protein 4,PDCD4)从而激活PI3K/Akt信号通路促进M2巨噬细胞的极化。
2.外泌体miR-29a-3P通过抑制SOCS-1/STAT6活性诱导M2巨噬细胞极化
在口腔鳞状细胞癌(Oral squamous cell carcinoma,OSSC)中,癌细胞衍生外泌体miR-29a-3p可以通过细胞因子信号转导抑制因子1(SOCS-1)/STAT6来调控巨噬细胞的极化。
3.外泌体 miR-25-3p、miR-130b-3p、miR-425-5p通过上调c-Myc诱导M2巨噬细胞极化
miR-25-3p、miR-130b-3p、miR-425-5p,同样可以通过外泌体从结直肠癌细胞转移到巨噬细胞,并且与miR-934相似,同样是通过Pten/PI3K/Akt途径来诱导巨噬细胞的M2极化。
4.豆状带绦虫囊尾蚴来源的miR-let-7c诱导M2巨噬细胞极化
骨髓间充质干细胞衍生的外泌体可以携带miR-let-7c,而有证据表明M2巨噬细胞的miRNA let-7c水平显著高于M1巨噬细胞,也就是说miR-let-7c可以促进M2巨噬细胞极化。还有一项研究发现豆状带绦虫囊尾蚴衍生的外泌体中同样可以携带miR-let-7c,并且可以通过靶向转录因子C/EBP δ继而促进M2巨噬细胞极化。
5 .miR-200b在肿瘤微环境中的不同作用
miR-200b会在卵巢上皮癌患者血浆衍生的外泌体中异常表达,并且可以通过下调PI3K/Akt信号通路抑制巨噬细胞的M2极化。但另一项研究发现miR-200b还可以通过抑制KLF6来调节巨噬细胞的极化。KLF6是一种高度保守的锌指蛋白,在恶性肿瘤中发挥肿瘤抑制因子的作用,并且研究发现KLF6可以抑制M2巨噬细胞的极化及其介导的肿瘤的增殖与迁移。也就是说miR-200b可以通过抑制KLF6促进M2巨噬细胞的极化从而促进上皮卵巢癌细胞的增殖和迁移。
6.外泌体诱导的M2巨噬细胞极化增强肿瘤耐药性
癌细胞衍生的外泌体诱导极化的M2巨噬细胞,已经在多项研究中被证明与肿瘤的发生发展与耐药性有关。在放疗,化疗,免疫疗法中,M2巨噬细胞可以通过影响肿瘤细胞的耐药性从而影响治疗效果:在非小细胞肺癌(NSCLC)细胞衍生的外泌体中发现了磷酸核糖焦磷酸合成酶 2 (PRPS2)的聚集,PRPS2可以通过介导M2巨噬细胞的极化促进肿瘤细胞对顺铂的耐药。在黑色素瘤中,Sulfasalazine与anti-PD-1/PD-L1联合治疗会降低anti-PD-1/PD-L1的疗效,出现这一现象的原因可能M2巨噬细胞极化有关。
7.外泌体PD-L1诱导M2巨噬细胞极化
外泌体携带的蛋白质同样在肿瘤微环境中发挥重要的作用。内质网(ER)应激的口腔鳞状细胞癌细胞可以释放富含PD-L1的外泌体,而这样的外泌体可以将ER的应激信号传递给浸润的巨噬细胞,从而促进M2巨噬细胞的极化。除此之外,外泌体PD-L1在肝癌中使肿瘤相关巨噬细胞高表达PD-L1,从而参与肿瘤免疫逃逸。
8.外泌体miR-33通过调整代谢诱导M1巨噬细胞极化
一项研究发现人乳腺癌衍生的外泌体携带的miR-33可以诱导巨噬细胞的M1极化,miR-33是一种代谢调节剂,在小鼠体内可以通过靶向MAPK途径减少脂肪酸氧化,促进M1巨噬细胞的极化,降低了乳腺癌细胞的侵袭性。这被认为与M1和M2巨噬细胞的代谢途径不同有关。
10.外泌体miR-9改变头颈部鳞状细胞癌对放疗的敏感性
人乳头瘤病毒(Human papillomavirus ,HPV)是头颈部鳞状细胞癌(Squamous cell carcinoma of head and neck,HNSCC)的诱发因素,但是HPV却可以促进HNSCC分泌外泌体,而HNSCC衍生的外泌体中就携带着丰富的miR-9。不过miR-9在肿瘤微环境中的作用,现在却出现了不同意见。有研究认为EGFR可以上调肿瘤微环境中miR-9的表达,通过靶向 KLF5,调节转录因子 Sp1 的表达,进而刺激肿瘤生长以及对放疗的抵抗;但另一项研究却认为HPV+ HNSCC衍生的外泌体携带的miR-9可以通过下调PPARδ的表达将巨噬细胞转化为M1表型,从而增加放射敏感性;其中PPARδ与配体结合时可以被激活并释放转录抑制因子bcl-6,抑制炎症基因的表达,与M1巨噬细胞的极化密切相关。另一项研究表明,M1巨噬细胞衍生的外泌体可以作为放疗的增敏剂,主要是因为M1巨噬细胞衍生的外泌体可以将M2巨噬细胞重新极化为M1巨噬细胞从而提高放疗效果[91]。除此之外,当M1巨噬细胞衍生的外泌体与gemcitabine合用治疗膀胱癌时同样可以提高化疗的治疗效果。
11.来源于短程照射DLD-1细胞的外泌体HMGB1诱导M1巨噬细胞极化
除了miRNA以外,研究者发现,当人结直肠癌上皮细胞(DLD-1)在经过短程照射后衍生的外泌体中可以携带高迁移率组蛋白1(High mobility group protein 1,HMGB1),而HMGB1在肿瘤微环境中可以诱导M2巨噬细胞向M1巨噬细胞转化。
12.外泌体THBS1诱导M1巨噬细胞极化
有研究发现血小板反应蛋白(Thrombospondin 1,THBS1)是OSCC外泌体含量最丰富的蛋白质,并被证实参与了巨噬细胞的极化,诱导巨噬细胞极化为M1表型。并且发现了这一过程取决于基于OSCC外泌体的癌细胞与肿瘤细胞之间的新型旁分泌环——通过p38、Akt 和 SAPK/JNK 等信号通路,巨噬细胞摄取OSCC 细胞释放的外泌体-THBS1被激活为M1表型。
最后文章提出了将外泌体作为肿瘤的治疗靶点,利用重编程巨噬细胞治疗肿瘤的潜力。巨噬细胞衍生的外泌体可以影响肿瘤的免疫逃避、耐药性等。由于来源于M1巨噬细胞的外泌体的抗肿瘤特性,使用药物调节巨噬细胞外泌体的产生以及利用巨噬细胞衍生的外泌体传递抗肿瘤药物成为了一种治疗肿瘤的可行思路。而目前于肿瘤微环境中外泌体的了解还不足以应用于临床,因为其发挥作用的原因和具体机制还尚未明确,与巨噬细胞的串扰关系也知之甚少。因此将肿瘤微环境中外泌体作为肿瘤的治疗靶点具有极大的临床意义与研究价值。
该课题受西南医科大学大学生创新创业项目支持。
韩云炜
王静
外泌体资讯网 BBA Rev Cancer | 西南医科大学附属医院王静、韩云炜团队发表综述:肿瘤微环境中的外泌体对巨噬细胞极化的影响