假体周围骨缺损是翻修全髋关节置换术(RTHA)中最严重的问题,容易导致假体与宿主骨之间的骨整合不足,最终导致假体松动。假体-宿主骨界面的骨髓间充质干细胞(BMSCs)和适度的炎症反应在骨整合中起着重要作用。RTHA假体大多采用钛合金(Ti6Al4V)制造,钛合金本身并不具备促进假体-宿主骨界面骨整合的生物功能。因此,有必要开发功能性假体,以加强假体-骨界面的骨结合,并降低假体松动率。近日,山东第一医科大学附属省立医院(山东省立医院)关节外科李伟教授团队在ACS Appl Mater Interfaces上发表题为“Exosome-Functionalized Ti6Al4V Scaffolds Promoting Osseointegration by Modulating Endogenous Osteogenesis and Osteoimmunity”的研究论文(doi: 10.1021/acsami.2c11102),介绍了该团队通过将S-Exos与聚乙烯亚胺(PEI)有效地固定在微弧形氧化物Ti6Al4V表面,构建的一种外泌体功能化的Ti6Al4V双重功能涂层(Ti-MAO@PEI-S-EXO)。该结构可通过同时调节BMSCs的BMP/Smad途径和巨噬细胞M2极化来促进骨整合。文章的第一作者为徐海伦,通讯作者为李伟教授与满振涛教授。
BMSCs是骨整合的重要种子细胞,可以转移到假体-骨界面并进一步分化为成骨细胞,启动骨整合过程。然而,由于直接引入外源性BMSCs存在一些缺陷,如方便性降低、排斥反应和区域性肿瘤发生,因此无细胞组织工程被认为是再生医学领域的一种安全和有效的策略。外泌体(Exos)是无细胞组织工程的重要载体,因为它们含有与母体细胞相似的蛋白质和RNA,并且可以通过直接的膜融合转移到目标细胞中。重要的是,有研究已经表明BMSC衍生的Exos通过调节成骨相关的miRNAs和蛋白质,促进BMSC的成骨分化。然而,在具有挑战性的环境中,如大型假体周围骨缺损,仅靠Exos不足以实现假体-骨界面的强大骨整合。因此,增强Exos的内在成骨诱导特性以促进骨结合可能是一种有前途的治疗策略。BMSCs的成骨诱导主要由BMP/Smad信号通路激活,然而,Smurf1可能会抑制BMSCs内的BMP/Smad信号通路,进一步阻碍其成骨分化。因此,该研究团队先构建了敲除Smurf1的工程化Smurf1-Exosomes(S-Exos),随后开发了一种Ti6Al4V表面的双重功能涂层(Ti-MAO@PEI-S-EXO),结果发现Ti-MAO@PEI-S-EXO可以通过同时调节BMSCs中的BMP/Smad途径和巨噬细胞的M2极化来有效增强假体-骨界面的骨整合。具体来说,Ti-MAO@PEI-S-EXO具有增强骨结合的双重功能,为改善RTHA中假体与宿主骨的骨结合提供了一种新的方法。
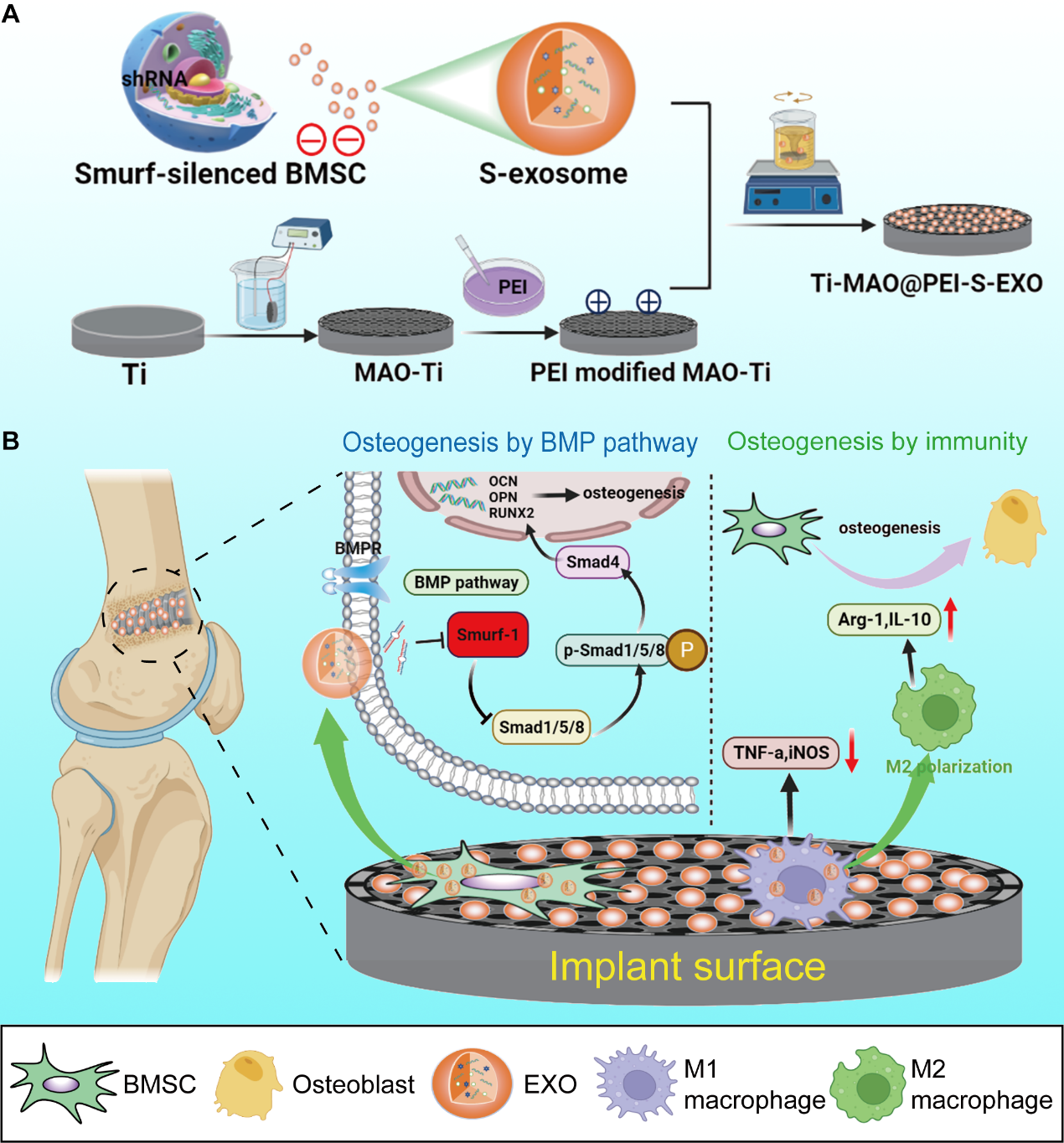
参考文献:Exosome-Functionalized Ti6Al4V Scaffolds Promoting Osseointegration by Modulating Endogenous Osteogenesis and Osteoimmunity, ACS Appl Mater Interfaces. 2022 Oct 6. doi: 10.1021/acsami.2c11102.
外泌体资讯网 ACS Appl Mater Interfaces | 山东第一医科大学附属省立医院李伟教授团队:外泌体功能化支架促进骨整合





