糖尿病患者循环中晚期糖基化终产物(AGEs)显著增加,并沉积于各组织器官,与糖尿病血管并发症显著相关。AGEs通过与AGEs受体RAGE结合激活内皮细胞(ECs),诱导活性氧产生,损害ECs,甚至诱导ECs凋亡。ECs是构成血管的第一道屏障,不仅参与运输营养物质并清除组织代谢产物,还分泌生物活性分子来调节细胞功能。研究表明内皮细胞一旦受到干扰,将分泌一些由细胞外囊泡携带的自我修复物质。激活或凋亡的内皮细胞产生的细胞外囊泡可以将蛋白质和miRNA递送给内皮细胞,以减少其凋亡并促进细胞修复。然而,激活或凋亡的内皮细胞产生的细胞外囊泡在糖尿病患者的血管钙化中对血管平滑肌细胞(VSMCs)钙化是否有影响尚不清楚。
近日,中南大学湘雅二医院代谢内分泌科、国家代谢性疾病临床医学研究中心袁凌青教授团队在Journal of Nanobiotechnology杂志上以Research Article 正式发表了题为“Protective role of small extracellular vesicles derived from HUVECs treated with AGEs in diabetic vascular calcification”的研究论文 (2022 Jul 16;20(1):334)。中南大学湘雅二医院袁凌青教授为该文通讯作者,2019级博士生郭孛为该文第一作者,中南大学湘雅二医院为论文唯一完成单位。
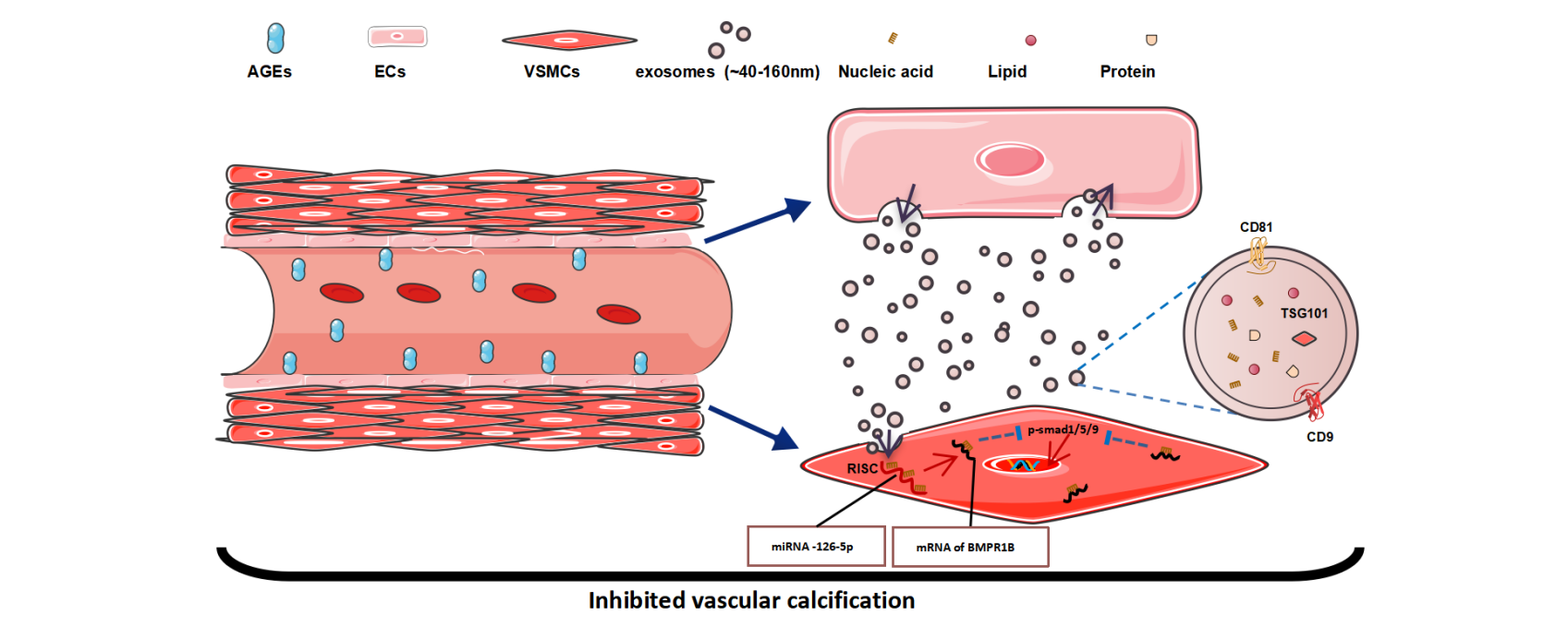
该团队首次发现了晚期糖基化终末产物(AGEs)刺激下血管内皮细胞和平滑肌细胞之间的一种崭新的通信机制。AGEs刺激人脐静脉内皮细胞(HUVECs)产生的细胞外囊泡可以减轻糖尿病小鼠的血管钙化。这一重要过程是通过细胞外囊泡富集的miR-126-5p实现的,其通过特异性靶向血管平滑肌细胞的骨形成蛋白受体(BMPR1B),阻断BMP-Smad信号轴,从而缓解血管钙化。该发现首次鉴定了细胞外囊泡富集的miR-126-5p是抗钙化的主要效应分子,进一步加深了对糖尿病动脉中膜钙化发病机制的理解,并为搭载miRNA的新型纳米药物递送治疗新靶点的开发提供了重要参考。
袁凌青教授团队长期致力于外泌体介导的血管病变机制及治疗研究。该团队将临床与基础科研紧密结合,做真正对患者有意义,对学术发展有推动的基础科研。参考文献:Protective role of small extracellular vesicles derived from HUVECs treated with AGEs in diabetic vascular calcification, . 2022 Jul 16;20(1):334. doi: 10.1186/s12951-022-01529-z.
外泌体资讯网 J Nanobiotechnology |湘雅二医院袁凌青教授团队:AGEs治疗的HUVEC细胞外囊泡对糖尿病血管钙化的保护作用





