外泌体是参与调节细胞间通讯的细胞衍生纳米囊泡,与传统的纳米药物相比,外泌体具有治疗开发的独特优势。来自美国南加州大学的研究人员设计了膜表面展示抗体靶向基团和免疫调节蛋白的基因工程化外泌体αCD3-αEGFR-PD-1-OX40L GEMINI-Exos,不仅可以激活T细胞杀死EGFR阳性的三阴性乳腺癌(TNBC) 细胞,而且还可以引发强大的抗肿瘤免疫。该研究发表于Molecular Therapy杂志上。
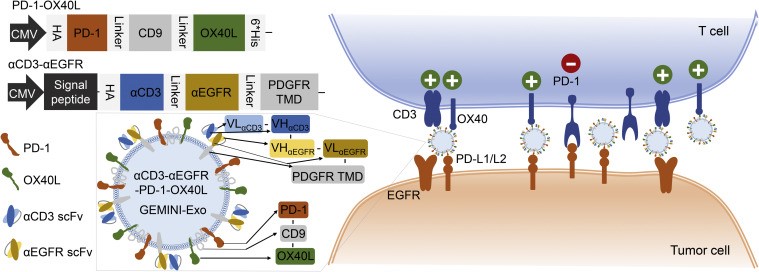
图. 用于靶向癌症免疫治疗的αCD3-αEGFR-PD-1-OX40L GEMINI-Exos示意图
外泌体是源自多种类型细胞的天然存在的膜状囊泡。外泌体的直径为30至150nm,携带大量来自亲代细胞的内容物。通过与细胞表面受体和配体的直接相互作用,或通过不同模式转移内容物质,外泌体能够调节受体细胞的生理学和病理生理学。这些纳米级囊泡是短距离和长距离细胞间通信的关键介质。作为纳米载体的天然形式,外泌体具有特征性的脂质双层膜和构成重要功能成分的膜蛋白。外泌体能够引导至靶细胞并与靶细胞膜融合,抑制机体的吞噬性清除,外泌体表面的蛋白质能够帮助细胞内容物递送并增加循环系统中的半衰期,这增强了外泌体的药理特性。包括出色的生物相容性,这些有价值的特征在开发外泌体作为一类纳米药物方面具有极大潜力。迄今为止,外泌体辅助药物递送在治疗各种人类疾病中显示出广泛的用途。但外泌体在免疫治疗中的潜力尚未得到充分利用。考虑到外泌体在细胞间通讯中的重要作用和独特优势,研究人员设想,在功能上重新编程这些细胞衍生的纳米囊泡,可能会产生一种创新形式的药剂,在激发疾病特异性的免疫反应方面具有有利的活性。与免疫检查点抑制剂和双特异性抗体等免疫疗法相比,外泌体可以在球形表面上实现免疫调节蛋白的多价表达。这将增加它们对免疫和患病细胞上的靶受体或配体的亲和力和结合力,并促进免疫突触的形成,从而增强免疫系统的激活。此外,针对不同信号通路的同一外泌体囊泡上的多种免疫调节蛋白的功能展示可能会促进协同作用,与传统的联合疗法相比,提供更好的治疗效果。为了证明这一假设,研究人员不仅展示了不同的免疫检查点调节剂,而且还使用遗传方法展示了外泌体表面上的靶向性。由 Expi293F 细胞产生的外泌体建立了基因工程多功能免疫调节外泌体 (GEMINI-Exos),其特征在于表面携带了程序性死亡蛋白1 (PD-1) 、OX40 配体(OX40L) 、T细胞CD3的特异性单克隆抗体和表皮生长因子受体 (EGFR,这是一种在许多人类癌症中经常过表达的受体酪氨酸激酶) 抗体。生成的αCD3-αEGFR-PD-1-OX40L GEMINI-Exos 对人CD3、EGFR、PD-1 配体和OX40具有很强的结合亲和力。使用三阴性乳腺癌 (TNBC) 的细胞和动物模型进行的临床前研究表明,αCD3-αEGFR-PD-1-OX40L GEMINI-Exos可以通过提高CD8+ T细胞的浸润,减轻调节性T细胞 (Tregs) 对EGFR阳性TNBC肿瘤的免疫抑制来诱导有效的细胞免疫。这项工作证明了基于GEMINI-Exos的癌症免疫治疗的临床前可行性,并为开发免疫治疗外泌体提供了基于基因工程的策略。
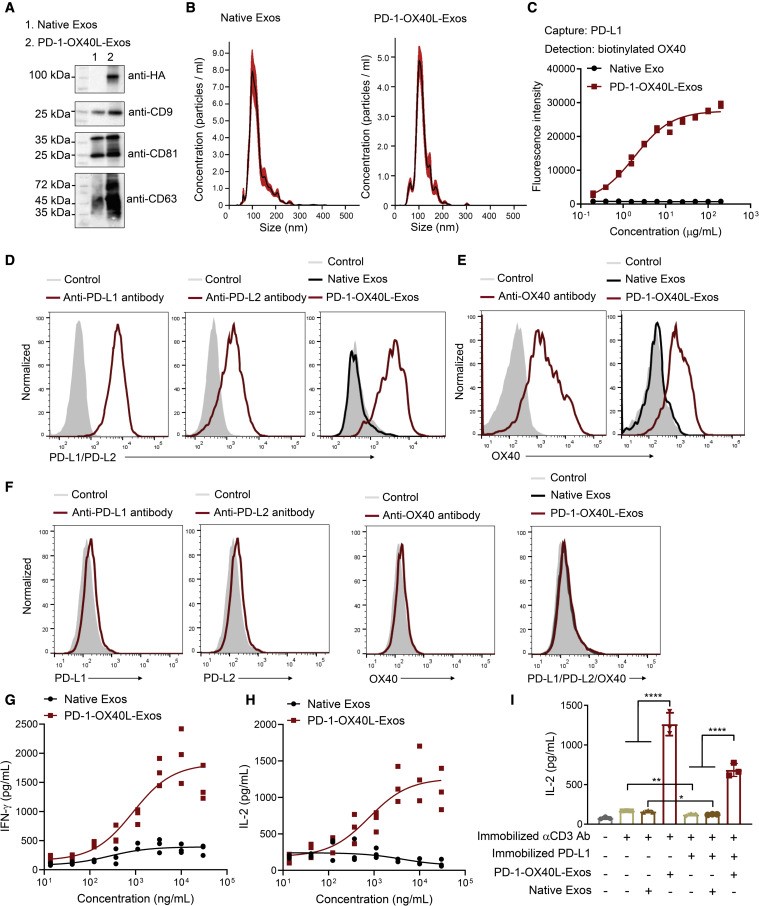
图:PD-1-OX40L-Exos的制备和表征。(A) 纯化外泌体的免疫印迹分析。 (B) 天然外泌体和PD-1-OX40L-Exos 的大小分布。 (C) PD-1-OX40L-Exos 与人PD-L1和OX40结合的夹心ELISA分析。(D-F) PD-1-OX40L-Exos 与 IFN-γ 刺激的BT-20 细胞 (D)、活化的人 T 细胞 (E) 和 MDA-MB-468 细胞(F) 结合的流式细胞术。(G-H)PD-1-OX40L-Exos对人类 T 细胞的剂量依赖性激活。(I) PD-1-OX40L-Exos 从 PD-L1 介导的抑制中恢复 T 细胞活化。
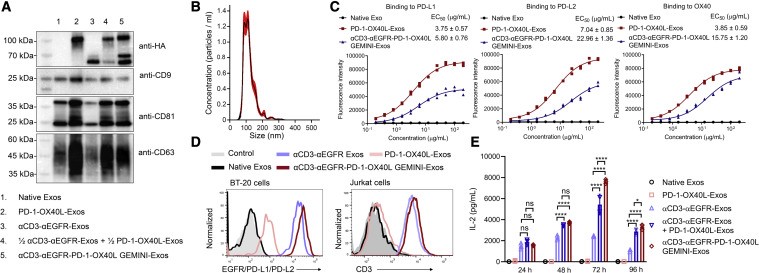
图:αCD3-αEGFR-PD-1-OX40L GEMINI-Exos 的产生和表征。(A) 纯化外泌体的免疫印迹分析。 (B) αCD3-αEGFR-PD-1-OX40L GEMINI-Exos 的大小分布。 (C) αCD3-αEGFR-PD-1-OX40L GEMINI-Exos 与人PD-L1、PD-L2 和 OX40 结合的 ELISA 分析。(D) αCD3-αEGFR-PD-1-OX40L GEMINI-Exos 与 BT-20 细胞 (EGFR+ PD-L1+) 和 Jurkat 细胞 (CD3+) 结合的流式细胞术。(E) αCD3-αEGFR-PD-1-OX40L GEMINI-Exos 对人类 T 细胞的时间依赖性激活。参考文献:Eliciting anti-cancer immunity by genetically engineered multifunctional exosomes. Mol Ther. 2022;S1525-0016(22)00373-2.