下腰痛(LBP)是全球最严重的医学和社会问题之一,已影响到全球近80%的人口,给受影响的个人和家庭带来了相当大的经济负担。而椎间盘退行性变(IDD)是一种常见的肌肉骨骼疾病,是LBP的主要诱因。IDD的病理基础包括细胞外基质(ECM)分解代谢和合成代谢的动态平衡受损,免疫级联反应失控激活,髓核(NP)细胞功能障碍和丢失,以及椎间盘微环境和动态细胞的生化改变。目前,IDD的主要治疗方法是手术治疗,然而外科干预只能缓解症状,却不能恢复固有的结构和功能。外泌体是直径为30-150 nm的囊泡,由干细胞、肿瘤细胞、免疫细胞和内皮细胞等多种细胞分泌;外泌体的脂质双层保护它们免受核糖核酸酶的降解,并有助于提高它们在受体细胞中的生物学效率。越来越多的证据表明,外泌体在诸多疾病中具有广阔的应用前景,并被认为是治疗IDD的潜在来源。
近日,空军军医大学西京医院骨科闫铭教授团队在Front CellDev Biol上发表了题为“Exosomes Immunity Strategy: A Novel Approach for Ameliorating Intervertebral Disc Degeneration”的综述文章(2022,10;9:822149),系统回顾了外泌体的来源及生物效应机制,包括外泌体的形成、外泌体的识别与鉴定、外泌体之间相互通讯的密切关系;以及外泌体通过抑制免疫微环境与炎症反应、抑制椎间盘血管化、促进ECM合成并抑制降解等途径缓解IDD的研究进展。空军军医大学西京医院骨科闫铭教授、高博副教授和首都医科大学潞河医院许崧杰副教授为本文通讯作者。空军军医大学西京医院骨科研究生李苇航、张世磊副教授及研究生王栋为本文共同第一作者。文章受到自然科学基金(82072475, 82172475)的资助。
该文详细介绍了外泌体在治疗IDD疾病中的具体机制及通路,包括干细胞来源(Stem cell-derivedexosomes)与非干细胞来源的外泌体(Non-stem cell-derived exosomes)。其中干细胞来源的外泌体又分为骨髓间充质干细胞(BMSC-exosomes)、人尿源间充质干细胞(USC-exosomes)、人胎盘间充质干细胞(PMSC-exosomes)以及脂肪源性间充质干细胞来源外泌体(ADSC-exosomes);而非干细胞来源的外泌体主要涉及髓核细胞(NP-exosomes)、纤维环细胞(AF-exosomes)以及脊索细胞来源的外泌体(NC-exosomes)。这些不同来源的外泌体在治疗IDD时相互协同或拮抗,共同调控IDD的变化。其中,PMSC-exosomes可能具有促进内皮细胞迁移以及管状形成的作用。PMSC外泌体调控IDD或内皮细胞功能的特异miRNAs以及它们的潜在作用还有待进一步鉴定。
越来越多的证据证实外泌体miRNAs在抑制NP细胞凋亡和抑制MMP表达中的作用,但该综述指出不同来源的外泌体及同种外泌体中不同的miRNA的表达差异及作用尚不清楚;椎间盘MSC-exosomes注射策略虽然显示了良好的效果,但关于MSC在临床实践中仍然存在障碍,特别是移植细胞如何能够在无血管的IVD条件下存活和适应;以及当使用类似于PMSC来源的外泌体时如何抑制血管生成而不是促进血管内长入椎间盘等,这些问题值得进一步思考与解决。
综上,该综述重点回顾并总结了不同来源的外泌体在缓解IDD疾病中的重要作用及现阶段关于外泌体治疗IDD存在的问题,为后续科研工作者的研究方向提供了指导。
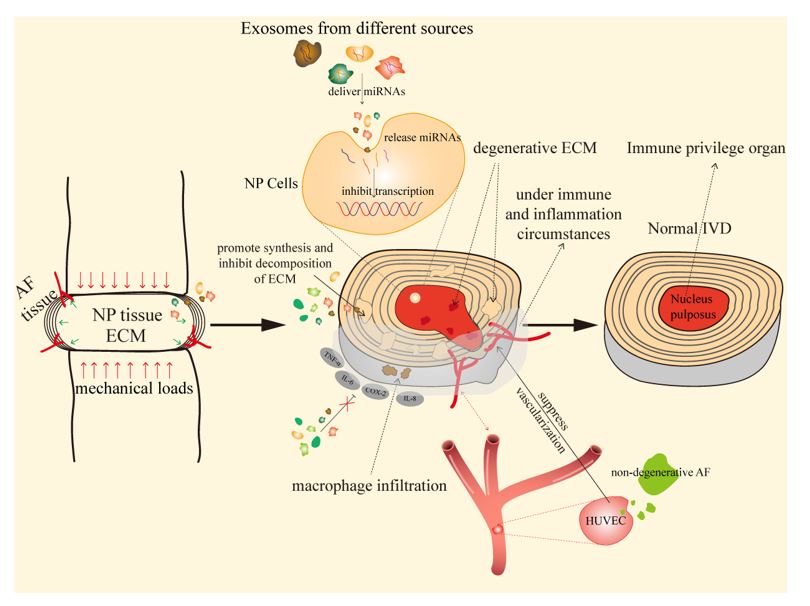
图1 外泌体治疗IDD模式图
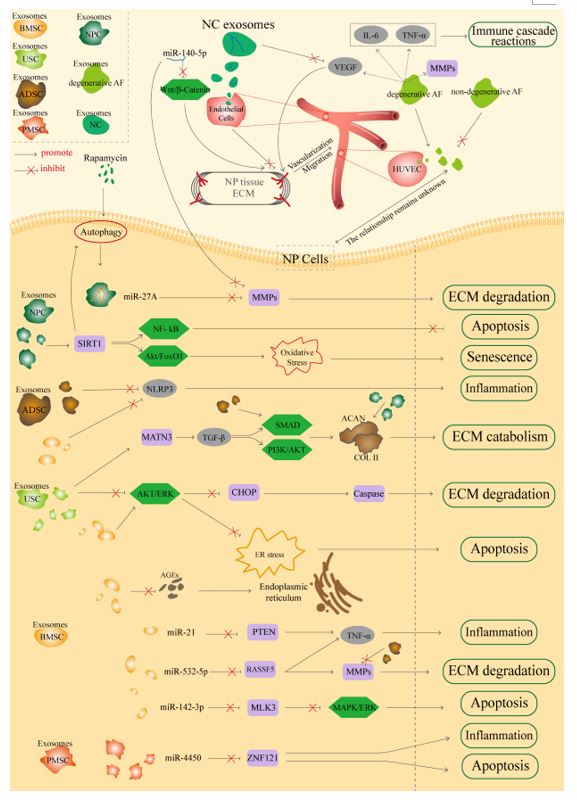
图2 不同来源外泌体治疗IDD的作用机制
参考文献:
Exosomes Immunity Strategy: A NovelApproach for Ameliorating Intervertebral Disc Degeneration. FrontCell Dev Biol. 2022,10;9:822149.
外泌体资讯网 Front Cell Dev Biol | 空军军医大学西京医院骨科闫铭教授团队:外泌体免疫策略:一种改善椎间盘退变的新方法