细胞外囊泡(EVs)是生物活性分子的纳米级生物载体,是细胞间通讯和治疗应用的新工具。EVs在临床前模型和早期临床试验中已显示出安全性和有效性。最近,来源于植物的细胞外囊泡样纳米颗粒(P-ELNs)因其在跨界递送包括核酸在内的治疗载荷方面的潜力而受到关注。来自生姜、柠檬、葡萄柚、葡萄和马齿苋的P-ELNs显示出治疗结肠炎的疗效。此外,P-ELNs已在酒精性肝炎和感染性疾病中显示出治疗潜力。P-ELNs具有生物相容性、生物可降解性、低免疫原性和可扩展性等优点,使其成为极具前景的药物递送载体。
2025年6月14日,广州医科大学王立富/杨宜/廖瑶团队在Journal of Nanobiotechnology(Top期刊,中科院1区,IF=12.6)在线发表了题为“Coptis chinensis-derived extracellular vesicle-like nanoparticles delivered miRNA-5106 suppresses NETs by restoring zinc homeostasis to alleviate colitis”的研究论文。该研究首次揭示了黄连来源的细胞外囊泡样纳米颗粒(Cc-ELNs)通过递送miR-5106调控锌稳态抑制中性粒细胞胞外诱捕网(NETs)的形成,从而缓解结肠炎的功能机制。这一发现不仅阐明了Cc-ELNs作为天然纳米颗粒在炎症性肠病(IBD)治疗中的新功能,还为基于植物源性纳米颗粒的免疫调节疗法提供了新靶点和新策略。广州医科大学金域检验学院博士后杨宜、硕士研究生杨兰梦茜为该论文共同第一作者。该研究得到广东省省企联合基金、广州市科技计划项目、广州市基础与应用基础研究项目、国家资助博士后人员计划、广州医科大学附属中医医院合作共建经费等项目资助。研究依托广州医科大学金域检验学院、广州医科大学医学检验大数据与经济研究所、广东省感染性疾病智能化诊断工程技术研究中心、广东省呼吸感染疾病预警和诊断工程技术研究中心、广州市传染性疾病临床快速诊断与预警重点实验室开展。动物实验依托于广州医科大学实验动物中心完成。广州医科大学金域检验学院为论文第一单位。
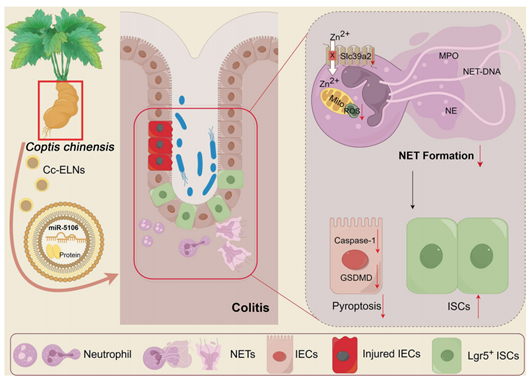
该研究发现,Cc-ELNs在DSS诱导的结肠炎模型中表现出显著的炎症靶向性,能够特异性地富集于肠道炎症部位。通过高通量测序和功能验证,研究团队鉴定出Cc-ELNs中高表达的miR-5106是其关键活性成分,该miRNA通过直接靶向中性粒细胞中的锌转运蛋白Slc39a2,有效调节细胞内锌离子稳态,从而显著抑制NETs的形成。在动物模型中,Cc-ELNs治疗不仅显著减轻了肠道炎症反应和病理损伤,还通过抑制NETs介导的肠道上皮细胞焦亡,促进肠道上皮屏障修复和干细胞增殖,展现出多方面的治疗优势。值得注意的是,研究还证实Cc-ELNs具有良好的生物相容性和安全性,在长期给药实验中未观察到明显毒副作用。这一发现不仅为理解植物源性纳米颗粒的跨物种调控机制提供了新视角,更为炎症性肠病的临床治疗提供了具有明确作用靶点的新型天然纳米药物策略,展现了中医药现代化研究的关键突破。
参考文献:
Coptis chinensis-derived extracellular vesicle-like nanoparticles delivered miRNA-5106 suppresses NETs by restoring zinc homeostasis to alleviate colitis. J Nanobiotechnology. 2025 Jun 14;23(1):444. doi: 10.1186/s12951-025-03466-z.
外泌体资讯网 J Nanobiotechnology|广州医科大学王立富/杨宜/廖瑶团队:黄连细胞外囊泡在炎症性肠病治疗中的应用





