颞下颌关节骨关节炎(TMJOA)是一种常见的退行性关节疾病,在全球的患病率为8%至35%,严重影响患者的生活质量。传统手术干预等治疗方法的效果有限,亟待开发再生性疗法。基于间充质干/基质细胞(MSCs)的治疗策略展现了巨大的潜力。其中,脂肪源性基质/干细胞(ASCs)因其获取容易及强大的增殖分化能力备受关注,已广泛应用于骨关节炎的临床试验并取得良好效果。然而,全细胞治疗仍面临安全性等问题,国内外研究者尝试开发其衍生物的替代疗法。
细胞外囊泡(EVs)具有与MSCs类似的生物学功能,但其作用机制有待进一步阐明。其中,EVs对免疫细胞的调控作用被认为是最关键的机制之一。树突状细胞(DCs)是免疫激活与耐受平衡的关键调控者,在骨关节炎发病和治疗中发挥核心作用。然而,ASC-EVs是否通过调控DCs发挥对TMJOA的治疗作用及其作用机制均不清楚。
重庆医科大学附属口腔医院李杰副教授团队在Journal of Nanobiotechnology杂志上发表题为“Extracellular vesicles from adipose-derived stromal/stem cells reprogram dendritic cells to alleviate rat TMJOA by transferring mitochondria”的论文,主要介绍了脂肪源性基质/干细胞的细胞外囊泡携带功能性线粒体结构传递至树突状细胞,使其发生代谢重编程至免疫耐受状态发挥对TMJOA的缓解作用。第一作者梅紫怡、李寒月,通讯作者李杰。

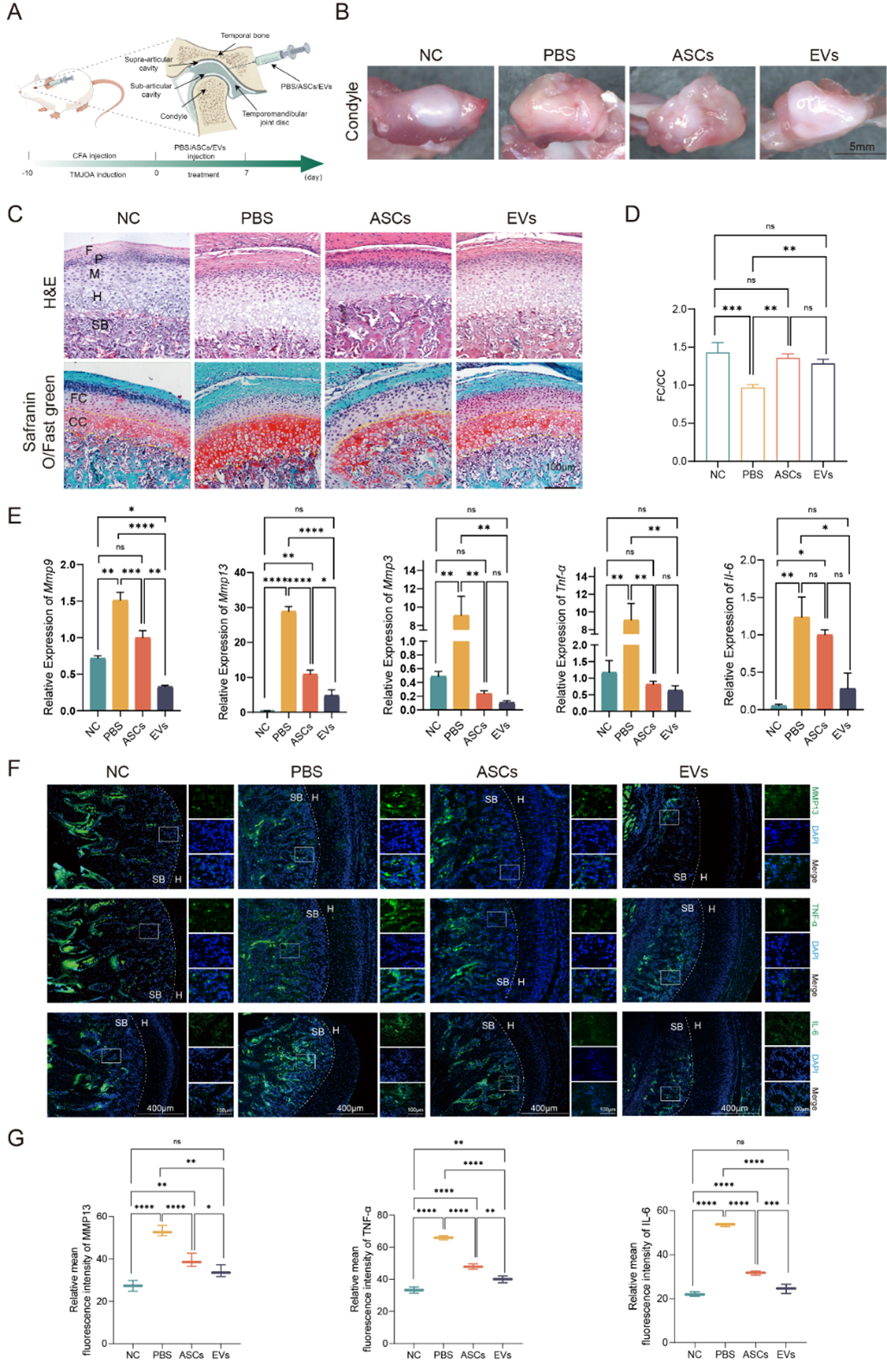
该研究发现通过关节腔内注射ASC-EVs与全细胞有相似的治疗效果,ASC-EVs可以减轻其疾病导致的炎症因子表达以及软骨损伤。
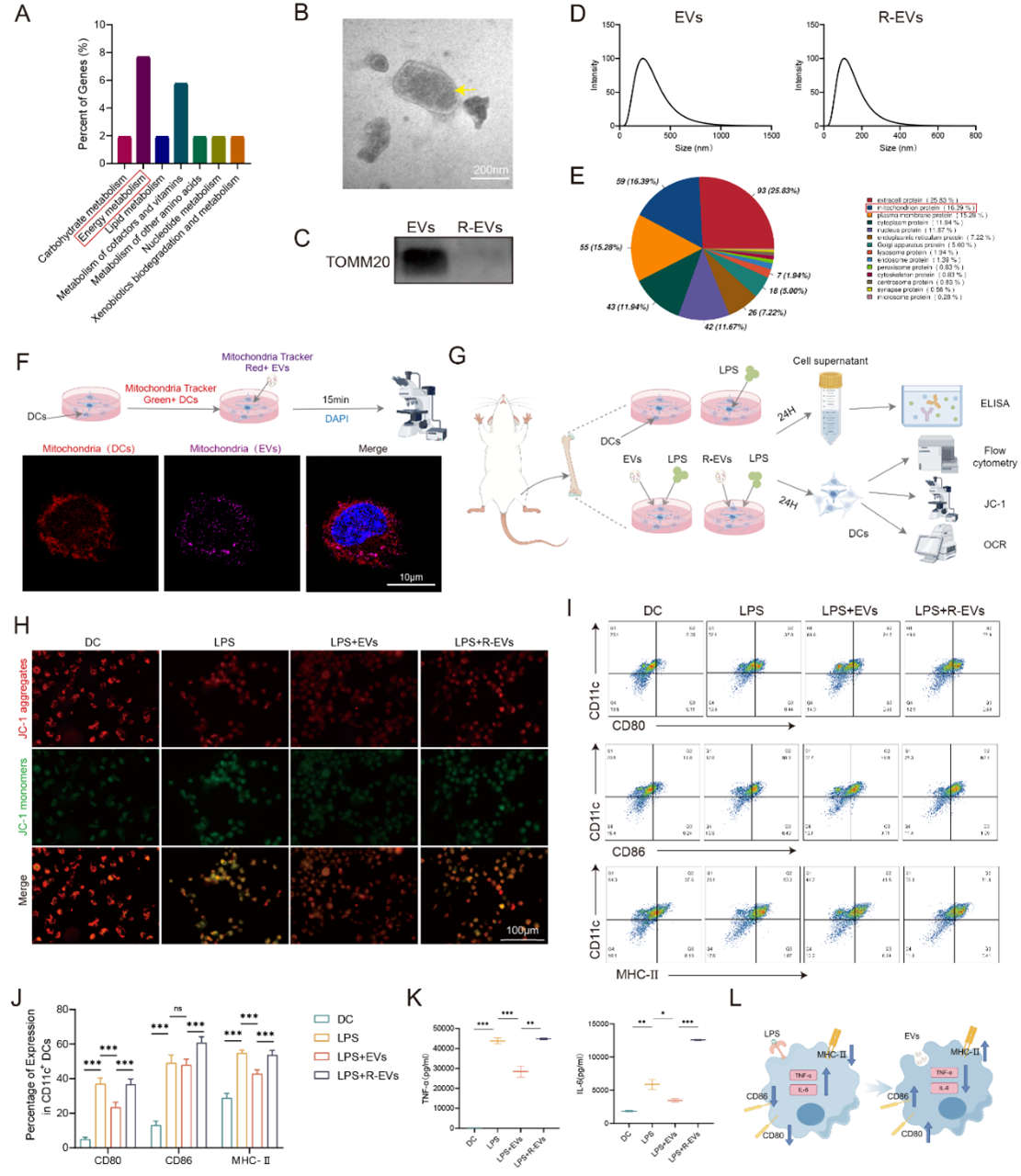
随后,研究人员发现ASC-EVs中存在线粒体结构,通过Rhodamine 6G处理抑制ASC-EVs的产生和功能后,显著降低了ASC-EVs对DCs成熟的抑制作用。表明ASC-EVs通过转移线粒体抑制了DCs的成熟。
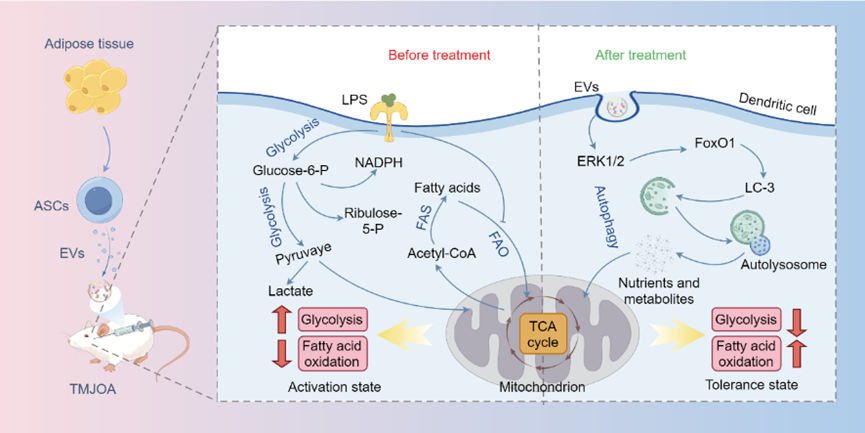
进一步通过转录组和代谢组学联合分析及一系列验证实验发现,ASC-EVs通过激活ERK1/2/FoxO1途径激活自噬从而实现对DCs代谢的重编程,进而缓解TMJOA的炎症及软骨破坏。该研究为ASC-EVs用于TMJOA的临床治疗提供了理论依据,同时也为其他疾病的治疗机制研究提供参考。
参考文献:
Extracellular vesicles from adipose-derived stromal/stem cells reprogram dendritic cells to alleviate rat TMJOA by transferring mitochondria. J Nanobiotechnol 23, 389 (2025). https://doi.org/10.1186/s12951-025-03478-9
外泌体资讯网 J Nanobiotechnol|重庆医科大学附属口腔医院李杰:脂肪源性细胞外囊泡通过转移线粒体减轻大鼠颞下颌关节骨关节炎