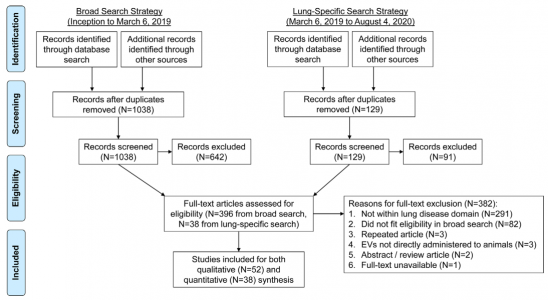
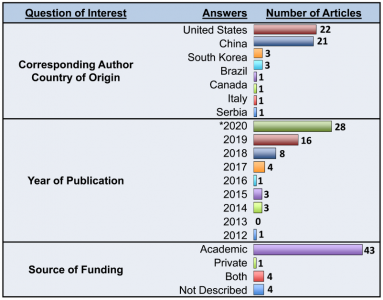
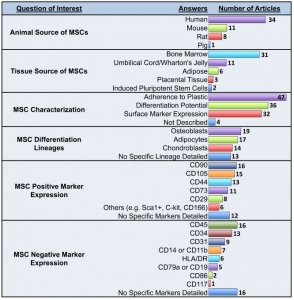
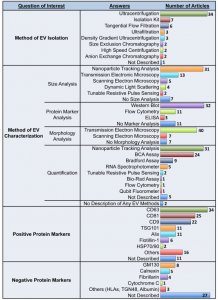
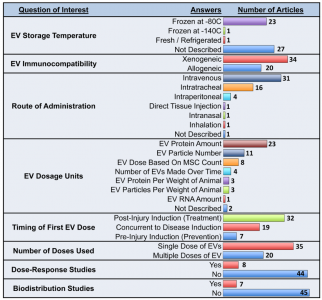
临床前研究表明间充质基质细胞胞外囊泡(MSC-EVs)可减轻炎症并改善肺部疾病的器官功能;然而,在临床转化之前需要对所有可用数据进行客观分析。近期JEV上的一篇文章对MSC-EVs治疗急性和慢性呼吸系统疾病进行了meta分析,综合统计分析了MSC-EVs对急性肺损伤(ALI;N=23)、支气管肺发育不良(BPD;N=8)和肺动脉高压(PAH;N=7)中不同分离技术和EV亚型等与治疗效果之间的关联。间充质基质细胞(MSCs)是一种异质细胞群,具有多能分化潜能和多种分泌、免疫调节和治疗功能。它们可以来自容易获得的组织,例如骨髓、脐带和脂肪组织。许多体外和体内研究表明,MSCs可以调节炎症通路、改善器官功能和延长生存期,目前在ClinicalTrials.gov上注册的临床试验超过1000项,研究MSCs作为对多种疾病的干预。尽管有这种广泛的兴趣,MSCs只获得了两种情况的批准,移植物抗宿主病和克罗恩病中的肛周瘘管。缺乏成功的临床转化是多因素的,但可能包括与产生一致、可行和有效的细胞疗法相关的技术挑战,例如,MSCs治疗中度至重度急性呼吸窘迫综合征的临床试验的事后分析表明细胞活力差别很大,从36%到85%。有趣的是,现在有人提出MSCs至少部分通过分泌细胞外囊泡(EVs)发挥其治疗作用,这可能代表比完整细胞递送更有效的治疗产品。呼吸系统疾病,无论是急性的还是慢性的,仍然是全世界死亡的主要原因。超过5亿人受到慢性肺病的影响,而治疗选择很少。此外,与COVID-19相关的急性呼吸窘迫综合征揭示了缺乏可用的特定疗法来对抗严重的呼吸道感染/损伤。鉴于MSC衍生的EV(MSC-EV)的抗炎和再生特性,肺部疾病已成为EV疗法临床前开发的重点。MSC-EVs的处理改善了急性(例如急性肺损伤,急性呼吸窘迫综合征的临床前相关模型)和慢性(例如肺动脉高压)疾病以及新生儿疾病(例如支气管肺发育不良)的结果。MSC-EV携带多种关键的mRNA、microRNA和蛋白质,这些已知可介导细胞过程,包括炎症、血管生成、细胞凋亡和纤维化,所有这些对肺恢复都至关重要。因此,EV可以潜在地利用全细胞的好处,同时克服许多伴随活细胞治疗的常见问题。这些优势包括EV可能具有较低的免疫原性、增强穿过重要生物屏障(例如肺内皮和上皮)的能力以及有利的制造/储存程序。随着EV疗法在过去十年中引起人们的兴趣,与开发这种无细胞疗法相关的挑战和悬而未决的问题仍然存在。该团队之前的系统综述中,分析了200多项研究MSC-EV作为治疗方法的体内研究的方法和结果。在EV命名、实验方法、干预特征、剂量方案和研究设计方面存在高度异质性。细胞外囊泡研究的最小信息(MISEV2018)试图解决其中的许多问题。然而,鉴于可用的EV方法的多样性,对于哪种分离技术、干预特征(例如MSC源或EV亚型)或给药方案(例如递送途径、治疗时间)将导致最大的治疗益处,尚无共识。在考虑临床转化之前,需要对这些实验细节以及MSC-EVs对肺修复的整体影响进行系统和全面的了解。在临床领域,科学严谨的系统评价和meta分析是客观、全面评估干预措施效果的金标准方法。它们客观地评估正在进行的研究的质量,阐明影响治疗结果的特定疗法或患者群体特征,并确定知识差距。通过在临床前EV研究中应用meta研究方法,该研究旨在确定MSC-EVs作为治疗各种急性和慢性呼吸系统疾病的疗效。完成了对急性肺损伤、支气管肺发育不良和肺动脉高压的meta分析。还进行了亚组分析,以探索可能与更大益处相关的特定EV特征和方法,以帮助改进MSC-EV治疗。最后,评估了目前存在于MSC-EV研究中的报告实验参数的质量和研究设计中偏倚风险。该文使用严格的meta研究方法确定了MSC-EVs对临床前呼吸系统疾病的有效性,并确定了可能进一步完善该疗法的实验条件。对MEDLINE/Embase的系统搜索确定了1167条记录。筛选后,纳入52篇文章进行数据提取,并评估研究设计中的偏倚风险和报告质量。对急性肺损伤(ALI;N=23)、支气管肺发育不良(BPD;N=8)和肺动脉高压(PAH;N=7)进行了随机效应meta分析。亚组分析确定了可能与提高疗效相关的EV方法/特征。数据以具有95%置信区间(CI)的标准化平均差(SMD)或风险比(RR)表示。对于ALI,MSC-EV显著降低肺损伤(SMD-4.33,CI-5.73至-2.92)、血管通透性(SMD-2.43,CI-3.05至-1.82)和死亡率(RR0.39,CI0.22至0.68)。小型EVs比大型EVs更一致有效,而在组织来源、免疫相容性或分离技术之间没有观察到差异。对于BPD,MSC-EV(SMD-1.45,CI-2.08至-0.82)改善了肺泡化,小EV比小/大EV更一致有益。在PAH中,EV显著降低了右心室收缩压(SMD-4.16,CI-5.68至-2.64)和肥厚(SMD-2.80,CI-3.68至-1.91)。在BPD和PAH中,通过超速离心分离的EV显示出相对更优的治疗益处,而切向流过滤(N=2)显示出最小的功效。最后,在所有研究中,实验设计的偏倚风险和报告质量始终不明确。研究结果表明,MSC-EVs在治疗急性和慢性肺病方面具有明显的潜力。然而,需要提高研究设计的透明度以及直接比较分离技术和EV亚型,以产生强有力的证据来指导临床转化。来自所有52篇肺病文章的一般研究特征概述,包括来源国、出版年份和资金来源。*2020年发表的MSC-EV肺研究数量是从纳入研究的总数中推断出来的。细胞外囊泡(EV)的干预细节。间充质基质细胞(MSCs)的组织和动物来源是从52篇纳入文章中提取的。对研究是否符合国际细胞治疗学会(ISCT)制定的MSC表征标准进行了评估。文章可能使用了来自不止一种动物和/或组织来源的EV。所用MSC的动物来源包括人(N=34;65%)、小鼠(N=11;21%)、大鼠(N=8;15%)和猪(N=1;2%)。MSC来源于多种组织来源,包括骨髓(N=31;60%)、脐带(N=11;21%)、脂肪组织(N=6;12%)、胎盘(N=3;6%)和诱导多能干细胞(iPSC)(N=2;4%)。研究用异种EV(N=34;65%)或同种异体EV(N=20;38%)。根据ISCT指南,30项研究(58%)符合MSC表征的所有三个标准。从52篇肺病文章中分离和表征细胞外囊泡(EV)的方法概述。记录使用的特定阳性和阴性蛋白质标记。研究可能在每个领域都采用了不止一种方法。EV分离最常用的技术是超速离心(N=34;65%)、分离试剂盒(N=7;13%)和切向流过滤(N=6;12%)。大多数研究EVs的特征在于量化(N=47;90%)、大小分布(N=45;87%)、形态分析(N=45;87%)和/或表面标记表达(N=41;79%)。根据MISEV2018指南,10项研究(19%)充分描述了他们的EV疗法。重要的是,52%(N=27)的研究没有报告对阴性标记的评估以证明EV的特定分离。关于EV命名法,该文评估了所使用的术语是否与报告的EV大小分布一致(例如,小型、大型或小型/大型EV组合)。35项(67%)研究使用一致的术语,而8项研究(15%)使用不一致术语,9项研究(17%)未提供大小分析。有关EV分离和表征的更多详细信息,包括使用的特定技术和标记,如上图。施用间充质基质细胞衍生的细胞外囊泡(MSC-EV)的给药方案。从52篇文章中提取了有关EV存储温度、给药途径、所用剂量单位、剂量数量、给药时间、生物分布分析和剂量反应研究流行率的详细信息。MSC-EVs用于肺部疾病的两种最常见给药途径包括静脉内(N=31;60%)和气管内(N=16;31%)递送。用于给药EV的单位差异很大,包括绝对蛋白质量(N=23;44%)、颗粒数(N=11;21%)或一定数量的MSC释放的EV量(N=8;15%)),以及随时间释放或按动物体重给药的EV。大多数研究提供单剂量治疗(N=35;67%);多次给药的研究使用了4个剂量的中值(范围为2-15个剂量)。在33项研究(63%)中进行了EV修改,其中包括EV分离前的修改(N=17;33%)、直接修改EV(N=8;15%)和联合治疗(N=8;15%)。最后,分别在8项(15%)和7项(13%)研究中检查了剂量反应和生物分布分析。Tieu A, Hu K, Gnyra C, Montroy J, Fergusson DA, Allan DS,Stewart DJ, Thébaud B, Lalu MM. Mesenchymal stromal cell extracellular vesiclesas therapy for acute and chronic respiratory diseases: A meta-analysis. JExtracell Vesicles. 2021 Oct;10(12):e12141. doi:10.1002/jev2.12141. PMID: 34596349.外泌体资讯网 MSC-EVs用于肺部疾病的分离方法等信息的meta分析