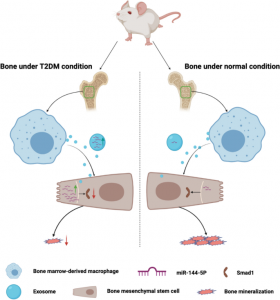
糖尿病患者存在着骨不连和骨折延迟愈合的风险,糖尿病环境如何影响巨噬细胞以及相关的成骨分化此前并不清楚。近日,来自武汉大学中南医院喻爱喜、简超课题组的研究人员发现,II型糖尿病环境下的骨髓来源巨噬细胞分泌的外泌体miR-144-5p,通过与骨髓间充质干细胞的通讯并靶向Smad1阻碍了骨折愈合和成骨分化,为治疗糖尿病骨折愈合受损提供有效的方法和潜在的治疗靶点。该研究发表于Journal of Nanobiotechnology杂志上。
糖尿病 (DM) 是人类的一个主要的健康问题,在全球范围内给个人和社会带来严重的医疗负担。不受控制的糖尿病会导致多器官病变,最终导致残疾并缩短预期寿命。在过去的几十年里,对动物和人的研究一致表明,糖尿病通过扰乱骨稳态平衡对骨折愈合产生不利影响,并且与非糖尿病患者相比,糖尿病患者骨折愈合时间延长一倍,延迟愈合和骨不连的风险更高。
人们越来越认识到,糖尿病受损骨的修复和再生被认为是巨噬细胞和骨髓间充质干细胞(BMSC) 之间异常通讯的结果,该通讯破坏了成骨分化和骨愈合。巨噬细胞广泛分布于体内,分泌多种生物活性物质、受体和酶,介导细胞间通讯,已被视为糖尿病并发症的一个重要方面。先前的研究表明,骨髓来源的巨噬细胞 (BMDM) 与 BMSC 紧密相邻,并通过分泌各种功能性生物分子来塑造骨微环境。此外,BMDMs已被证明在糖尿病引起的不良病理状态下,分泌IL-1、TNF-α、iNOS等成骨受阻因子,从而损害成骨分化并增加骨折修复不受控制的可能性。然而,这些因素既不能完全代表糖尿病疾病下的巨噬细胞-骨髓间充质干细胞间的联系,也不能完全解释糖尿病患者在糖尿病条件下骨修复和再生受损的潜在机制。
外泌体是通过各种细胞类型分泌的直径为 50-100 nm 的细胞外囊泡,来源于内体,可以携带丰富的生物活性物质,如非编码RNA、mRNA、DNA、蛋白质等分子。最近的研究表明,外泌体通过传递含有特定 miRNA 的货物来有效地介导细胞间和器官间的通讯。一些miRNAs已被揭示通过在转录后水平调节靶基因的表达参与骨髓间充质干细胞增殖、迁移、分化和凋亡的调控,表明miRNAs是骨修复和再生的重要调节因子。有证据表明,外泌体miRNAs 能够从骨微环境稳定转移到 BMSCs 中,有助于成骨分化和骨折愈合过程。因此,外泌体 miRNA 是骨折修复的关键调节因子,在修复过程的各个阶段具有重要作用。事实上,一些研究表明,来自巨噬细胞的外泌体 miRNA 能够在体内外影响BMSC 分化以及骨折愈合。然而,BMDM衍生的外泌体 miRNA 的影响、对糖尿病的作用以及它们与 BMSC间的通讯仍未确定。
在这项研究中,研究人员评估了糖尿病环境对BMDM衍生的外泌体miRNAs的体外和体内的改变、与BMSCs 的细胞间通讯的改变、以及对成骨分化和骨折修复的影响。体内外的实验发现,与非糖尿病的骨髓来源的巨噬细胞分泌的外泌体(nBMDM-exos)相比,糖尿病骨髓来源的巨噬细胞分泌的外泌体(dBMDM-exos)的成骨潜力和骨折修复能力较低。有趣的是,dBMDM-exos 中 miR-144-5p 水平急剧升高,并且可以转移到 BMSC 中通过靶向 Smad1调节骨再生。此外,dBMDM-exos 对成骨潜能和骨折修复能力的不利影响可以通过抑制miR-144-5p而被逆转。这些结果证明了外泌体 miR-144-5p 在骨再生中的重要作用,为开发改善糖尿病患者骨折愈合的新策略提供了见解。
参考文献;MiR-144-5p, an exosomal miRNA frombone marrow-derived macrophage in type 2 diabetes, impairs bone fracturehealing via targeting Smad1. J Nanobiotechnology. 2021 Jul 30;19(1):226.