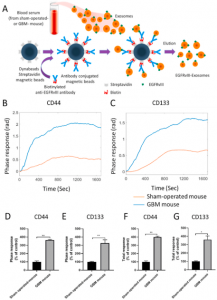
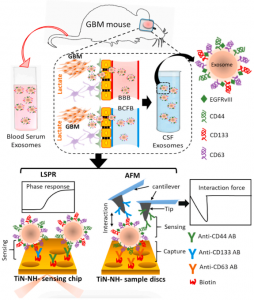
胶质母细胞瘤(GBM)是一种致命的脑肿瘤,其分泌的乳酸增强CD44的表达和外泌体(细胞来源的30-200 nm纳米囊泡)的释放,从而促进肿瘤恶性进展。近日,香港城市大学的LEE Youngjin (李永鎮)教授和Lawrence WU(胡志文)教授在Biosens Bioelectron杂志(影响因子10.618)上发表文章,报道发现乳酸驱动的恶性胶质母细胞瘤(GMs)中CD44上调增强了富含CD44的外泌体的释放,从而增加了GMs的迁移和内皮细胞的管形成,并且分泌的外泌体中的CD44可通过“捕获和传感”氮化钛 (TiN) -纳米孔 (NH) -圆盘免疫捕获 (TIC)-原子力显微镜 (AFM) 和超灵敏的TiN-NH局部表面等离子体共振 (LSPR) 生物传感器灵敏检测。中枢神经系统 (CNS) 中最常见的致命肿瘤是恶性胶质母细胞瘤 (GBM),其进展的特点是GBM细胞(GMs)的迁移和侵袭增加以及内皮细胞 (ECs) 的管形成增强。恶性GBM患者的平均生存期仅为一年半,部分原因是其早期诊断困难,以及与迁移、侵袭和血管生成相关的糖酵解重编程进展迅速。由于糖酵解增强,即使有足够的氧气供应,恶性GM会产生大量乳酸并将其释放到肿瘤微环境 (TME) 中,这被称为“Warburg 效应”。TME中增加的乳酸已被证明会扩散到肿瘤相关的成纤维细胞中,并刺激透明质酸 (HA) 的合成和释放,从而进一步增强GMs和ECs与重组细胞外基质(ECM)的粘附,导致肿瘤生长。有趣的是,还发现高水平的乳酸显著上调GMs中的CD44,这是一种细胞表面粘附分子,并通过与ECM中配体HA的相互作用进一步促进其迁移和侵袭。重要的是,当GMs增强表皮生长因子受体变体 III(EGFRvIII)(一种肿瘤特异性致癌蛋白)的表达时,CD44显著上调并分布在GMs的丝状伪足膜中,从而增加了它们的迁移和侵袭。因此,已经很好地证明了HA、CD44的水平及其相互作用与肿瘤严重程度呈正相关。此外,HA-CD44 相互作用的抑制剂已显示出抗癌作用,从而进一步表明它们的相互作用在肿瘤进展中是必不可少的。最近的报告也清楚地表明,患者组织中HA和CD44的水平可以作为追踪肿瘤恶性程度的精确生物标志物。除了CD44,一种重要的癌症预后生物标志物,CD133,也已被证明在富含乳酸的缺氧肿瘤中被上调。外泌体是最小类型的细胞衍生细胞外囊泡 (EV),大小范围为30-200 nm,存在于大多数生物体液中,包括血液和脑脊液 (CSF),它们在正常和病理条件下的细胞-细胞通讯中发挥重要作用,例如GBM。越来越多的证据表明,恶性GM部分通过代谢重编程和乳酸将大量外泌体释放到细胞外环境中,通过增强与周围细胞的自体和异源相互作用来支持肿瘤存活。特别是,跨越血脑屏障(BBB)和血脑脊液屏障(BCSFB)的GMs衍生外泌体可用作生物标志物发现平台来追踪其来源GMs的恶性进展。.最近,分子谱分析也证实了外泌体成分,包括外泌体microRNA和蛋白质,是检测肿瘤恶性时的重要生物标志物。因此,用于外泌体生物标志物的无创和微创无标记生物传感技术已被认为是肿瘤诊断和预后的有前途的方法,因为它们可以简单地定量测量与特定类型癌症及其恶性进展相关的表面蛋白。在这些技术中,临床上可用的表面等离子体共振 (SPR) 生物传感器已被利用,并在外泌体蛋白的灵敏检测中表现出出色的性能。例如,基于金纳米岛 (AuNI) 的局部 SPR (LSPR)、基于金膜的SPR和基于金纳米棒的LSPR已被应用于检测CD63,一种特定的外泌体标记物。金在SPR传感中很受欢迎。然而,其较差的物理稳定性会随着长期重复使用而降低生物传感的准确性和灵敏度。为了解决这个问题,氮化钛(TiN)由于具有低电阻率、耐腐蚀性、可调光吸收、高显微硬度、化学和热稳定性等特性而被用作替代等离子体材料。例如,芯片上的TiN纳米膜涂层有助于调整可见光谱中的等离子体特性,芯片上的单个TiN涂层可提供较低的限制损失而没有物理不稳定性。为了提高检测性能,采用了新的基于纳米的方法,例如等离子体材料合金和核壳结构,并证明可以增强芯片的等离子体传感特性。此外,通过在芯片的TiN纳米薄膜上引入纳米孔,对表面电磁波进行局部化和放大,进一步提高了检测灵敏度。因此,这项研究解决了具有强定位表面等离子体激元的TiN-NH-LSPR生物传感器是否可以产生足够灵敏的LSPR响应来精确检测血液和脑脊液中的微量外泌体蛋白。原子力显微镜 (AFM) 还可以灵敏地检测和量化样品盘上捕获的外泌体表面蛋白与其功能化配体或氮化硅悬臂尖端上的抗体 (AB) 之间的单分子相互作用力。 例如,AFM力谱(AFM FS)通过抗原-AB相互作用灵敏地量化了癌症衍生的外泌体中的生物标志物水平。为了开发更好的生物标本圆盘,已经测试和使用了各种AFM基板圆盘材料。在这些材料中,云母、ap-云母、玻璃、石墨、硅和金已被应用于构建生物样本盘。最近的研究结果表明,TiN也可以成为捕获具有生物相容性的生物样本的绝佳材料。它可以直接吸收生物素化的AB,使外泌体能够被捕获在圆盘上,以便对生物标志物进行进一步的单力分析。因此,需要解决是否可以使用基于TiN的AFM圆盘来实现外泌体生物标志物的“连续捕获和传感”。来自GBM小鼠模型血清的EGFRvIII-ABs免疫捕获的GMs衍生的外泌体中CD44和CD133水平增加该研究首先证明了乳酸刺激GMs的外泌体通过CD44对迁移和血管生成增强的影响,以及来源GMs的恶性状态与其外泌体中CD44水平之间的密切正相关。特别是,证明了新建立的无标记TiN-NH-LSPR生物传感器可以灵敏地检测来自GBM小鼠模型的血液和脑脊液的外泌体中增加的CD44、CD133、EGFRvIII水平,使用EGFRvIII ABs进一步验证了这一点。免疫捕获的GMs衍生的外泌体,为开发基于外泌体的敏感生物传感技术提供了很好的见解,用于检测早期GBM形成并进一步监测GBM进展,作为一种液体活检方法。使用TIC-AFM-和TiN-NH-LSPR-生物传感器检测外泌体CD44的外泌体极限浓度分别为5.29×10-1 μg/mL和 3.46×10-3 μg/mL。重要的是,这项工作首次发现无标记的灵敏TiN-NH-LSPR生物传感器可以检测和量化GBM小鼠模型血液和脑脊液中免疫捕获的GMs外泌体中增强的CD44和CD133水平,支持在GBM进展的微创分子诊断中作为液体活检的潜在应用。TIC-AFM和TiN-NH-LSPR生物传感器超灵敏检测外泌体CD44和CD133的代表图,以跟踪小鼠GBM的进展ThakurA, Xu C, Li WK, Qiu G, He B, Ng SP, Wu CL, Lee Y. In vivo liquid biopsy forglioblastoma malignancy by the AFM and LSPR based sensing of exosomal CD44 andCD133 in a mouse model. Biosens Bioelectron. 2021 Jul2;191:113476. PMID: 34246124.外泌体资讯网 香港城市大学:AFM和LSPR检测外泌体CD44和CD133,恶性胶质母细胞瘤的液体活检