胰腺导管腺癌(PDAC)的预后是所有癌症中最糟糕的一种,诊断后PDAC患者的中位生存期仅为6-8个月。虽然数十年的研究工作一直集中在早期诊断和分子机制的理解上,但很少有临床上有用的标记物得到普遍应用。为了改善PDAC的治疗和管理,确定最佳治疗决策和患者生存的预后因素同样重要。令人信服的证据表明,细胞外囊泡(EV)可能用作PDAC的非侵入性生物标志物。近日,J Hematol Oncol杂志上的一篇文章报道确定基于血浆的非侵入性EV生物标志物,以预测PDAC患者手术后的存活率。
胰腺导管腺癌(PDAC)约占胰腺癌的90%,是公认的男性和女性最致命的癌症之一,全球死亡率极高。PDAC患者诊断后的中位生存率仅为6-8个月,5年总生存率仍然低至11%。PDAC的性质在分子、病理和临床水平上具有异质性,这使得改善生存的机会有限,因此治疗进展和预后信息受到影响。例如,基因组特征、大规模转录组分析产生的分子亚型、世界卫生组织(WHO)分类的组织学亚型和疾病进展模式已被尝试用于治疗和预后应用,但结果较少比令人满意的。因此,为了优化治疗分层和管理,发现用于预测PDAC患者生存的特异性和敏感但非侵入性的生物标志物仍然存在重大未满足的临床需求。
在寻找此类生物标志物时,循环细胞外囊泡(EV)作为液体活检的高潜力来源已成为研究的焦点。它在PDAC的背景下特别有吸引力,因为原发肿瘤本身的取样是一种侵入性方法,具有感染和扩散肿瘤细胞的风险。大量研究表明EV货物作为PDAC临床应用的潜在生物标志物的潜力。例如,与年龄匹配的健康对照相比,更高百分比的PDAC患者在其循环EV衍生DNA中表现出可检测到的突变KRAS,这与局部疾病患者的无病生存率降低有关,表明诊断和预后潜力EV衍生的DNA。除此之外,循环血浆EV中的一组蛋白质货物(例如BAIAP2L1、ALPL、PTPRJ、FCER1G和TMEM2),或单一血清衍生的EV蛋白Glypican-1和/或与其他蛋白质标记EGFR、EpCAM的组合,来自PDAC患者的MUC1和WNT2已被描述为具有高准确性和敏感性的早期癌症检测的生物标志物。至于RNA,迄今为止的大部分研究都集中在microRNA(miRNA)、长RNA(主要是信使RNA、长链非编码RNA和环状RNA)和转移RNA(tRNA)作为诊断和预后癌症生物标志物。特别是,来自血浆EV的一组长RNA(FGA、KRT19、HIST1H2BK、ITIH2、MARCH2、CLDN1、MAL2和TIMP1)已成功验证用于PDAC的早期诊断,曲线下面积(AUC)为0.936,表明来自EV的长RNA作为诊断因素的潜力优于目前PDAC的诊断标记,碳水化合物抗原19-9(CA19-9)。尽管快速发展的EV研究领域取得了令人鼓舞的成果,但值得注意的是,循环EV的mRNA在PDAC预后应用中的潜在作用在很大程度上尚未得到探索。
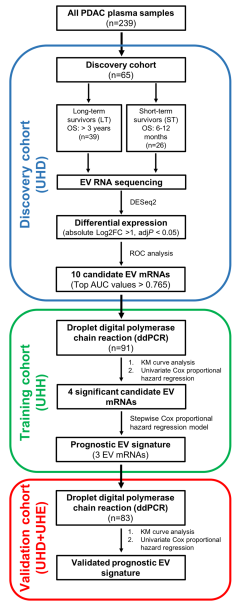
该研究的目的是确定非侵入性EV mRNA生物标志物,以预测PDAC患者手术后的存活率。据推测,血浆EV含有mRNA货物,可用作PDAC患者生存预测的预后生物标志物。通过检查发现队列中长期和短期PDAC幸存者的血浆EV转录组,并在另一个PDAC患者训练队列中测试选定的候选者,该研究确定了预后EV 3-mRNA特征。EV特征允许在训练和验证队列中对PDAC患者进行风险分层,与低风险组相比,高风险组的总生存率(OS)降低。重要的是,这种EV3-mRNA特征在与肿瘤分期相结合时显示出优异的预后性能,表明它可以作为当前预后因素的补充。此外,单变量和多变量分析表明,EV3-mRNA特征是PDAC预后的独立不利预测因子。这些数据表明,血浆EV mRNA可以作为生物标志物,通过无创风险分层预测PDAC患者的OS。本研究的基本目标是通过深入了解PDAC与血浆EV mRNA的预后来填补当前的EV研究空白,突出一个有很多值得探索的新兴领域。
方法:从总共258名PDAC患者中分离出血浆EV,分为三个独立的队列(发现、训练和验证)。RNA测序首先用于通过DESeq2工具从发现队列(n=65)中识别差异表达的EV mRNA候选者。候选者通过数字液滴聚合酶链反应(ddPCR)在训练队列(n=91)中进行了测试。Cox回归模型和Kaplan-Meier分析用于构建EV特征,随后通过ddPCR在多中心队列(n=83)上进行验证。
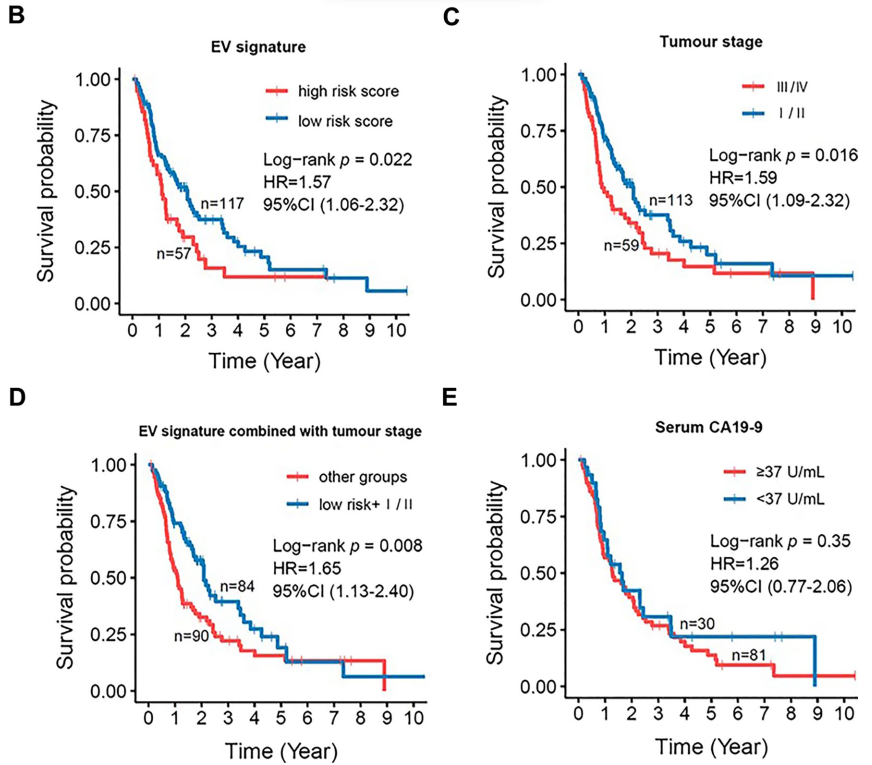
结果:血浆EV的转录组学分析揭示了长期和短期PDAC幸存者之间差异表达的mRNA,这导致10个排名靠前的候选EV mRNA在一个独立的训练队列中使用ddPCR进行了测试。ddPCR的结果能够建立一个新的预后EV mRNA特征,由PPP1R12A、SCN7A和SGCD组成,用于PDAC患者的风险分层。根据EV mRNA特征,与训练队列中的低风险患者相比,高风险PDAC患者的总生存率(OS)降低(p=0.014),这在另一个独立队列中得到了成功验证(p=0.024)。有趣的是,该特征和肿瘤分期的组合产生了比单独的特征(p=0.022)或肿瘤分期(p=0.016)更好的预后表现(p=0.008)。值得注意的是,EV mRNA特征被证明是PDAC预后的独立不利预测因子。
EV 3-mRNA特征是PDAC患者总生存期(OS)预测的独立预后生物标志物
该研究为PDAC患者的风险分层和生存预测提供了一种新的非侵入性预后EV mRNA特征。
参考文献:
Han Y, Drobisch P, Krüger A, William D, Grützmann K, Böthig L, Polster H, Seifert L, Seifert AM, Distler M, Pecqueux M, Riediger C, Plodeck V, Nebelung H, Weber GF, Pilarsky C, Kahlert U, Hinz U, Roth S, Hackert T, Weitz J, Wong FC, Kahlert C. Plasma extracellular vesicle messenger RNA profiling identifies prognostic EV signature for non-invasive risk stratification for survival prediction of patients with pancreatic ductal adenocarcinoma. J Hematol Oncol. 2023 Feb 3;16(1):7. doi: 10.1186/s13045-023-01404-w. PMID: 36737824; PMCID: PMC9896775.