表达嵌合抗原受体(CAR)的基因工程T细胞正在迅速发展,有望用于血液学和非血液学恶性肿瘤的治疗。CAR-T疗法可引起快速而持久的临床反应,但常出现急性毒性等副作用。
来自第二军医大学基础医学部胡适课题组的研究人员发现,CAR-T细胞会释放表面表达CAR的外泌体,含CAR的外泌体能显著抑制肿瘤生长并且安全性较好,是一种潜在的新的抗肿瘤治疗方法。该研究发表于Nature Communications杂志上(IF=11.878)。
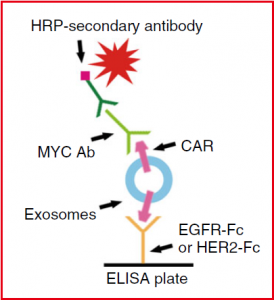
图:CAR-T细胞分泌的外泌体表面CAR的表征
基于嵌合抗原受体(CARs)或T细胞受体(TCRs)的基因工程自体细胞、或同种异体T细胞作为细胞免疫疗法的应用正在成为一种有前景的新治疗方法。该方法利用广泛细胞毒性的特异性T细胞去靶向治疗癌细胞。CAR由靶结合域和跨膜信号域组成,靶结合域是由CAR-T细胞特异性表达的细胞外域,跨膜域是信号传导域,是向T细胞提供激活信号的细胞内域。CARs的靶向特异性通常是通过抗原识别区域以单链可变片段(scFv)或胞外域中的结合受体/配体的形式实现的,而T细胞激活功能是通过胞内结构域实现的。在当前的临床开发中,针对CD19 + B细胞的恶性肿瘤,包括急性和慢性B细胞白血病和B细胞非霍奇金淋巴瘤(NHL),抗CD19的CAR-T细胞是最先进的过继性T细胞免疫疗法之一,并已获得FDA批准。在单机构进行的众多I / II期临床试验数据表明,对于标准疗法难治的B细胞恶性肿瘤,这种方法通常可使总体缓解率达到50-90%。
尽管效果显著,但过继性T细胞疗法仍显示出一些毒性,这种毒性与常规化学疗法、单克隆抗体(mAb)和小分子靶向疗法所见的毒性不同。随着这些免疫疗法的应用增加,对毒性的认识至关重要。CAR-T免疫疗法中最常见的两种毒性作用是细胞因子释放综合征(cytokine release syndrome,CRS),其特征是高烧、低血压、缺氧或多器官毒性;以及CAR-T相关性脑病综合征(CAR-T-related encephalopathy syndrome,CRES),通常以毒性脑病状态为特征,其表现为妄想症、神志不清,偶尔还有脑水肿和癫痫发作。罕见出现的暴发性噬血细胞淋巴组织细胞增生症(HLH)(或巨噬细胞激活综合征,MAS)的病例通常以严重的免疫激活、淋巴组织细胞浸润和免疫介导的多器官功能衰竭为特征。其他的一些重定向T细胞疗法,例如TCR基因疗法和双特异性T细胞结合抗体(BiTE),以及临床前CAR自然杀伤细胞,都能够诱导这种毒性。尽管在治疗难治性血液系统恶性肿瘤患者中观察到CAR-T细胞有强烈应答,但在实体瘤中的结果却比较有限。这可能是由于实体肿瘤的肿瘤微环境(TME)中存在着许多障碍,比如由上调抑制性受体(IR)介导的内在抑制途径引起治疗不佳,这些抑制受体对CAR-T细胞在肿瘤中的同源配体例如PD1信号等会发生反应。
外泌体属于细胞外囊泡(EVs)的一个亚型,在体内大多数细胞都可以分泌。根据EV的生物发生的不同,EV可分为三个亚组,包括外泌体(直径为30-150 nm)、微囊泡(150-1000 nm)和凋亡小体(50-2000 nm)。近来,证据表明EV可能作为细胞间通讯的介质发挥关键作用。外泌体在这些囊泡中受到了最多的关注,并且也已得到充分表征。此外,关于人类T细胞来源的外泌体,它们在细胞毒性T淋巴细胞(CTL)和靶细胞的相互作用中的重要作用在先前的研究中得到了验证。CTL衍生的外泌体包含CTL表面膜分子(CD3、CD8和TCR),从而确保将杀伤性内容物单向递送至目标肿瘤细胞。TCR与适当的抗原/MHC组合之间相互作用的共轭形成导致靶细胞死亡。目标细胞的杀伤作用是由外泌体中的致命化合物(包括颗粒酶、溶酶体酶和穿孔素)诱导的。TCR激活可促进CTL衍生的外泌体的产生,另一项相关研究还证明了TCR /CD3ζ复合物在人CTL分泌的外泌体膜中存在。
基于外泌体的生物学特性,源自CAR-T细胞的外泌体在免疫治疗中具有直接攻击的作用。因为外泌体与类似于脂质体的合成药物载体具有功能和结构上的相似性,所以外泌体可以进一步用于药物递送。但是,由于CAR-T细胞的靶向特异性是由CAR结构中抗体衍生的scFv决定的,因此直接从CAR-T细胞培养基中分离的外泌体可能具有异质性,并且可能失去靶向特异性。这些数据表明,源自CAR-T细胞的纯化含CAR外泌体可用作癌症靶向剂,并可以改善现有的治疗效果。
在这项研究里,研究人员发现由CAR-T细胞释放的外泌体在其表面上携带有CAR。含CAR的外泌体表达高水平的细胞毒性分子,并被用作肿瘤治疗。体外和临床前体内模型的分析表明,CAR外泌体不表达PD1,并且重组PD-L1处理并不能削弱CAR外泌体的抗肿瘤作用。在细胞因子释放综合征的临床前体内模型中,与CAR-T治疗相比,CAR外泌体的给药相对更加安全。因此,这些数据证实外泌体可用作仿生纳米囊泡,这可能是治疗癌症的新的有效策略。
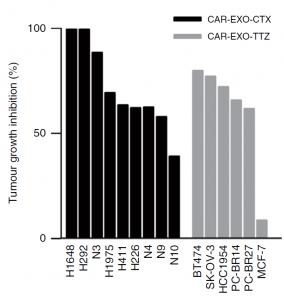
图:CAR-T细胞分泌的外泌体的体内抗肿瘤效果
参考文献:Fu W, Lei C, Liu S, Cui Y, Wang C, Qian K, Li T, Shen Y, Fan X, Lin F, Ding M, Pan M, Ye X, Yang Y, Hu S. CAR exosomes derived from effector CAR-T cells have potent antitumour effects and low toxicity. Nat Commun. 2019 Sep 25;10(1):4355.