作者:吴迪
近日,来自Uppsala University的中国学者吴迪博士在Nature 子刊 Nature Communications 杂志(IF 11.880)上发表题为“Profiling surface proteins on individual exosomes using a proximity barcoding assay”的文章,提出了一种分析单外泌体表面蛋白的新技术—邻近编码技术(Proximity Barcoding Assay,PBA),该技术通过抗体DNA偶联物和新一代测序分析单个外泌体的表面蛋白组成。
外泌体(exosome)是细胞多泡内体与质膜融合时释放产生的微小囊泡,广泛存在于生物体液中。外泌体作为传递生物信息的载体,参与调控重要的细胞生理活动,在免疫应答、血管生成、炎性反应等生理病理过程中均发挥一定作用。外泌体膜上携带有亲代细胞来源的表面蛋白,反映其来源细胞的生理、病理及功能状态,可作为疾病生物标志物。具有诊断意义的外泌体表面蛋白标志物在样本中可能由于其丰度太低而无法被检测,为此,文章中提出了一种灵敏度高、特异性好的单外泌体分析技术,可实现外泌体的异质性研究。
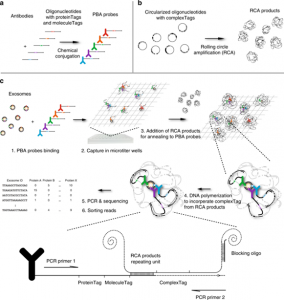
PBA技术的设计和工作流程
在PBA中,研究人员使用微米大小的单链DNA簇,每个簇具有数百个通过滚环扩增产生特有的DNA拷贝序列,可对单个外泌体进行DNA编码标记。样本中单个外泌体的表面蛋白组成通过与之结合的抗体-DNA偶联物可被转化为DNA序列信息,该偶联物合并了每个滚环扩增产物中重复的随机编码序列。通过PCR扩增后,利用新一代测序技术解析DNA序列中包含的蛋白和外泌体信息,以识别单个外泌体的表面蛋白组成。在此基础上,作者们使用链霉亲和素-生物素-寡核苷酸复合物进一步证明了PBA分析单个外泌体的能力。
外泌体蛋白的定量分析和单个外泌体可视化聚类
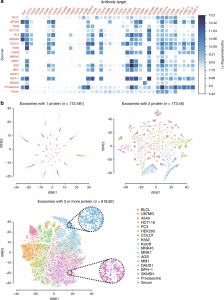
本研究利用PBA技术对来自18种不同来源的外泌体膜上38种不同表面蛋白进行分析(图a),样本来源包括人血浆、人前列腺液以及16种细胞系培养上清中的外泌体。在对单外泌体表面蛋白定量后,经过深度学习分析,每一个单外泌体的膜蛋白组被两两比较相似度,分别按照1种、2种、3种或更多表面蛋白组合特征被分成亚群,展示于t-SNE图中(图b),研究结果表明,通过识别更多的表面蛋白组合可更好地区分不同来源的外泌体,PBA技术能解析出每个单外泌体上蛋白的种类和个数,不同蛋白的共表达,即以表面蛋白的组合形式作为生物标志物。
邻近编码技术可高通量地编码标记样本中所有单外泌体表面蛋白,其检测限度取决于蛋白结合特异性、测序的范围和深度、以及抗体的亲和力和选择性。通过比较不同来源的外泌体图谱,可找到特定的表面蛋白组合作为生物标记物,用于识别和量化从健康和疾病的特定组织释放进入血液中的外泌体。
PBA 技术文章:Wu et al. (2019) Profiling surface proteins on individual exosomes using a proximity barcoding assay, Nature Communications, DOI: 10.1038/s41467-019-11486-1