土豆
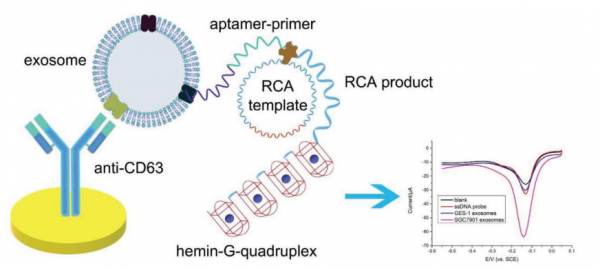
图:高灵敏度检测外泌体的无标记电化学适体传感器示意图
胃癌细胞的外泌体通过调节肿瘤微环境增强肿瘤迁移和侵袭能力,但目前检测肿瘤特异性外泌体仍然是一个很大的挑战,大多数方法都无法在正常外泌体的背景中有效检测肿瘤来源的外泌体。近日,来自南京大学医学院附属鼓楼医院检验科李智洋老师和东南大学生物电子学国家重点实验室何农跃老师开发了一种无标记的电化学适体传感器用于胃癌外泌体的特异性检测。该研究发表于Small杂志(IF 9.598)上。
胃癌是癌症死亡的第二大原因,在全球癌症死亡相关原因中排名前列。据统计,2012年新诊断胃癌病例数为951.6万例,死亡人数为723.1万例。80%的胃癌患者在最初诊断时已经是晚期,导致胃癌的总体5年生存率很低。因此,迫切需要早期诊断胃癌的新方法,制定更有效的治疗策略并降低死亡率。
外泌体是由几乎所有类型的细胞通过质膜融合而分泌的纳米级磷脂双层囊泡。外泌体中含有生物分子,包括蛋白质、脂质和核酸,如mRNA、microRNA和DNA片段等。外泌体在细胞间通讯和疾病进展中发挥重要作用。最近的研究证明,胃癌细胞分泌的外泌体可能有助于胃癌的病理过程,促进肿瘤的生长、迁移、侵袭和化疗抗性。外泌体存在于各种体液中,并且具有特定的分子特征,这于它们的来源细胞特征相关。外泌体被认为是癌症的潜在诊断生物标志物。目前已经开发了许多方法实现了外泌体的定量,包括流式细胞术、纳米粒子追踪分析、酶联免疫吸附测定与微流体平台结合、以及电化学生物传感器等。核酸适配体(aptamers)是一种可以特异性结合相应靶标的短的ssDNA或者RNA分子。外泌体跨膜蛋白特异的核酸适配体和抗体通常可以用作外泌体的检测探针。然而,外泌体在临床实践中的应用仍然具有挑战性,目前可用的大多数检测探针一般是CD63特异性适配体或者是抗CD63抗体。由于CD63通常存在于外泌体中,包括疾病相关的外泌体和正常外泌体,因此在患者机体中存在着高水平的正常CD63“生物噪音”。电化学适体传感器(electrochemical aptasensors)由于其简单、低成本和对样品体积较小的要求,在外泌体检测领域具有很大的优势。电化学适体传感器采用不同的信号生成和扩增策略,如DNA纳米四面体、金属纳米粒子和基于核酸的扩增分析。然而,一些核酸扩增分析需要高温条件下进行,这会影响外泌体完整性。滚环扩增(Rolling circle amplification,RCA)是一种新型核酸扩增技术,能够产生高分子量产物以实现信号放大。由于RCA反应可在室温下进行,因此该技术非常适用于生物样品的检测。到目前为止,RCA尚未应用于外泌体检测。
在这项研究中,研究人员报道了一种无标记的电化学适体传感器,通过将hemin / G-quadruplex系统和RCA结合起来,实现选择性和灵敏地检测胃癌外泌体。首先,研究人员筛选了几种胃癌细胞或几种肿瘤类型中过表达的蛋白质适配体,选择了胃癌外泌体特异性的适配体。然后用抗CD63抗体修饰的金电极中捕获不同种类的外泌体。在这些外泌体中,只有胃癌外泌体可以通过RCA实现大量G-quadruplex的产生。然后将产物与hemin一起孵育以形成hemin / G-quadruplex结构,并最终催化H2O2产生电化学信号。该适体传感器对胃癌外泌体具有高选择性和灵敏度,检测限为9.54×102个外泌体/毫升,线性响应范围为4.8×103~4.8×106个外泌体/毫升。因此,该电化学适体传感器有望成为胃癌早期诊断的有用工具。
参考文献:Huang R, He L, Xia Y, Xu H, Liu C, Xie H, Wang S, Peng L, Liu Y, Liu Y, He N, Li Z. A Sensitive Aptasensor Based on a Hemin/G-Quadruplex-Assisted Signal Amplification Strategy for Electrochemical Detection of Gastric Cancer Exosomes. Small. 2019 Apr 8:e1900735.
外泌体资讯网 南京大学&东南大学:基于Hemin / G-Quadruplex辅助信号放大系统的适体传感器用于胃癌外泌体的电化学检测