转移是肺癌死亡的主要原因,骨髓来源的间充质干细胞(BMSC)是肿瘤微环境的重要组成部分并且促进肿瘤进展。近日,来自中南大学湘雅医学院向娟娟课题组、中南大学湘雅二医院唐敬群课题组的研究人员发现,BMSC衍生的外泌体miRNA介导缺氧肿瘤微环境中的细胞与细胞间通讯,并通过激活STAT3信号通路诱导EMT途径进而促进肺癌细胞的侵袭。该研究发表于Molecular cancer杂志上(IF 7.776)。
肺癌是癌症相关死亡的主要原因之一。外泌体是一种含有蛋白质和RNA的细胞外膜囊泡,其分子组成稳定并具有组织特异性,可以反映其来源组织的病理生理状态。在外泌体中已被鉴定出很多mRNA和微小RNA(miRNA)种类。miRNA是19-22nt的非编码RNA,可通过外泌体的隔离保护避免循环miRNA的降解。在外泌体中特定miRNA水平的增加与癌症进展相关。外泌体是细胞与细胞间通讯的主要介质,因为外泌体可被相邻细胞所捕获。外泌体介导的特定miRNA从基质细胞向上皮肿瘤细胞的转移有助于癌症进展。外泌体由许多细胞分泌,可以在体液中检测到,包括血液、尿液和支气管肺泡分泌物,这些都被认为是生物标志物的理想来源。对于外泌体miRNA在癌症发展中的作用,特别是在癌症进展的非侵入性检测中,有很好的应用前景。
肿瘤细胞和微环境细胞会受到一系列压力因素的影响,如缺氧、代谢应激、饥饿、氧化应激等。缺氧是实体瘤的一个显著特征。肿瘤细胞的快速生长速度超过了氧气的输送速度,就会产生局部缺氧。大多数实体瘤具有永久或短暂地缺氧的区域。缺氧会增强肿瘤细胞的含有CD63和CD9的外泌体的释放。除此之外,环境中的氧分压也可以改变外泌体的含量。
骨髓间充质干细胞(BMSCs)是一种多能基质细胞,被募集到肿瘤附近并促进肿瘤进展。虽然骨髓被认为是一种供氧量较低的组织类型,但实体瘤组织中心的氧含量甚至更低,接近0.025 kPa(0.1-0.2%的氧气浓度)。骨髓间充质干细胞所在的微环境与骨髓微环境、肿瘤微环境是存在差异的。在本研究中,研究人员使用microRNA阵列进行外泌体miRNA谱分析,并利用肺癌细胞和小鼠体内肿瘤模型评估几个外泌体miRNA的效果。同时利用缺氧BMSC衍生的血浆外泌体miRNA在癌症患者和健康对照之间、转移和非转移的肿瘤患者之间进行区分和鉴别。
结果发现,来自缺氧BMSCs的外泌体被邻近的肿瘤细胞摄取,促进肿瘤细胞侵袭和EMT过程。外泌体介导的一些特定miRNA(包括miR-193a-3p、miR-210-3p和miR-5100)从BMSC向上皮肿瘤细胞的转移激活了STAT3信号传导并增加EMT相关分子的表达。单一miRNA具有准确的区分度,比如血浆外泌体miR-193a-3p可以区分癌症患者和非癌症对照。三种血浆外泌体miRNA比单独一种miRNA更好地区分转移和非转移肺癌患者。因此,研究人员认为,外泌体介导的miR-193a-3p、miR-210-3p和miR-5100的转移可通过激活STAT3信号诱导的EMT促进肺癌细胞的侵袭,这些外泌体miRNA可能是肿瘤进展有前景的非侵入性生物标志物。
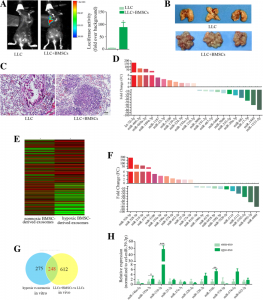
图:缺氧培养的BMSC分泌的外泌体中miRNA的鉴定及其促进肿瘤侵袭的能力
参考文献:Zhang X, Sai B, Wang F, Wang L, Wang Y, Zheng L, Li G, Tang J, Xiang J. Hypoxic BMSC-derived exosomal miRNAs promote metastasis of lung cancer cells via STAT3-induced EMT. Mol Cancer. 2019 Mar 13;18(1):40.