肿瘤相关巨噬细胞促进了肿瘤的发生和发展。来自华中科技大学同济医院王桂华、胡俊波课题组在Cancer Research杂志发表论文,揭示了肿瘤微环境中M2型肿瘤相关巨噬细胞诱导结肠直肠癌细胞的迁移和侵袭的新机制,为转移性结直肠癌的治疗提供了新思路。
肿瘤相关巨噬细胞(Tumor-associated macrophages,TAM)是肿瘤微环境中促进肿瘤进展的主要参与者和协调者。通常,巨噬细胞可以极化为M1型或M2型巨噬细胞。 M1极化的巨噬细胞被细胞因子如IFNγ激活,并产生促炎和免疫刺激细胞因子(如IL12、TNFα等)。然而,TAM被认为更接近M2极化巨噬细胞,其由Th2细胞因子(IL4、IL10和IL13)激活。据报道,随着肿瘤的进展,TAMs可以促进肿瘤细胞的增殖、侵袭和转移,刺激肿瘤相关的血管生成,并抑制抗肿瘤免疫应答。随着TAM与肿瘤之间关系的逐渐被阐明,TAM现在被认为是肿瘤的潜在治疗靶点。然而,TAM促进癌症转移的机制以及TAM与肿瘤细胞之间的通讯模式仍待探索。
近年来,外泌体的功能得到了广泛关注。外泌体是来源于自多泡体的脂质双层膜囊泡(50-100nm),其通过与细胞膜融合而释放。外泌体已被认为作为介导肿瘤细胞和微环境细胞通讯的关键因素。也就是说,外泌体在促进肿瘤生长、肿瘤发生、肿瘤血管生成、肿瘤免疫逃逸、耐药性和转移中起重要作用。特别是,外泌体已被用作肿瘤诊断的有希望的生物标志物,甚至作为肿瘤患者的潜在治疗靶标。
在这项研究中,研究人员发现M2型巨噬细胞调节的结直肠癌细胞的迁移和侵袭依赖于M2巨噬细胞衍生的外泌体(macrophage–derived exosomes,MDE)。MDE中表现出miR-21-5p和miR-155-5p的高表达水平,并且MDE介导的结直肠癌细胞的迁移和侵袭均依赖于这两种miRNA。在机制上,miR-21-5p和miR-155-5p通过MDE转移至结直肠癌细胞并与BRG1编码序列结合,下调BRG1的表达,而BRG1在转移性结直肠癌细胞中下调,是一种确定的促进结直肠癌转移的关键因子。总之,这些发现表明M2巨噬细胞诱导结肠直肠癌细胞的迁移和侵袭,并且在肿瘤恶性进展期间分泌外泌体穿梭到结直肠癌细胞,靶向和下调BRG1表达。结直肠癌细胞和M2巨噬细胞之间的这种动态和相互联系为转移性结直肠癌的治疗提供了新的机会。
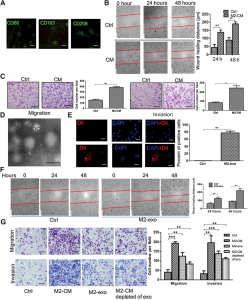
图:M2巨噬细胞分泌的外泌体促进结直肠癌细胞的侵袭转移
参考文献:Lan J, Sun L, Xu F, Liu L, Hu F, Song D, Hou Z, Wu W, Luo X, Wang J, Yuan X, Hu J, Wang G. M2 Macrophage-Derived Exosomes Promote Cell Migration and Invasion in Colon Cancer. Cancer Res. 2019 Jan 1;79(1):146-158.
外泌体资讯网 Cancer Research:华中科技大学王桂华、胡俊波课题组发现M2巨噬细胞来源的外泌体促进结肠癌细胞迁移和侵袭