乳腺癌作为全球女性健康的重大威胁,其转移过程是导致患者预后不佳的主要原因。细胞外囊泡(EVs)在肿瘤微环境(TME)中扮演着“特洛伊木马”的角色,深度参与肿瘤的发生、发展、转移及治疗抵抗,揭示其机制对改善乳腺癌预后至关重要。
辽宁省肿瘤医院康悦教授团队联合沈阳工业大学白石教授团队在Molecular Cancer杂志上发表题为“Extracellular vesicles: the“Trojan Horse” within breast cancer host microenvironments”的综述论文,深入探讨了细胞外囊泡在乳腺癌病理发生机制中的作用以及其作为潜在治疗干预手段的前景。 第一作者是康悦副教授,通讯作者为沈阳工业大学白石教授。
肿瘤微环境(TME)由一个复杂的网络组成,涉及肿瘤细胞、非癌细胞以及它们产生和释放的一系列分子。其组成部分包括细胞外基质、癌症相关成纤维细胞、炎症免疫细胞、肿瘤相关血管以及由这些细胞实体排出的EVs。 在TME中,EVs发挥着类似于 "特洛伊木马 "的作用,对肿瘤的发生、发展、转移以及对治疗干预的反应产生重大影响。源自肿瘤细胞和TME内相关实体的EVs可促进以下过程:刺激肿瘤部位附近的血管生成,在远处的解剖区域建立预转移龛,诱导癌细胞发生转化性变化,从而获得促进侵袭、血管生成、免疫逃避、远处转移和抗化疗的特性。值得注意的是,EVs 因其固有的生物相容性而具有穿越生物屏障的独特能力,使其成为创新药物输送系统的理想候选物质。这一特性为突破传统癌症治疗的限制提供了一条途径。该研究深入探讨了 EVs 在乳腺癌中的致病机制,并研究了前瞻性的治疗干预措施,为即将推出的针对乳腺癌的精确制导疗法奠定了基础。
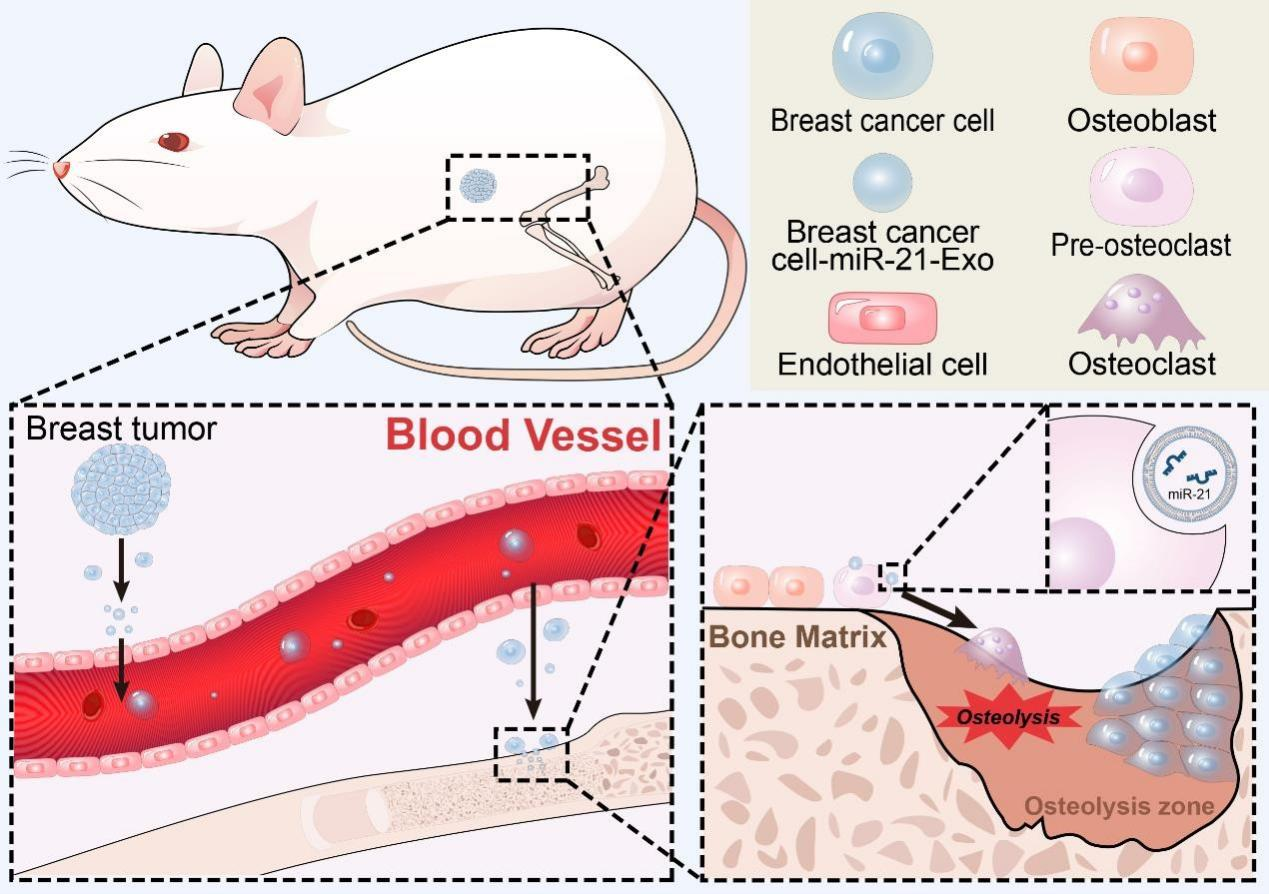
1、EVs通过miRNA介导的信号通路促进乳腺癌骨转移前微环境的形成
研究发现,乳腺癌细胞(bccs)释放的富含mir-21的外泌体被破骨细胞前体摄取,通过增加nfatc1的表达和降低pdcd4的水平,促进破骨细胞分化和骨溶解。而富含mir-19a的外泌体可抑制pten表达,激活nf-κb和akt信号路径,进一步增强破骨细胞发育和骨溶解活性,从而促进循环肿瘤细胞在骨骼中的植入。
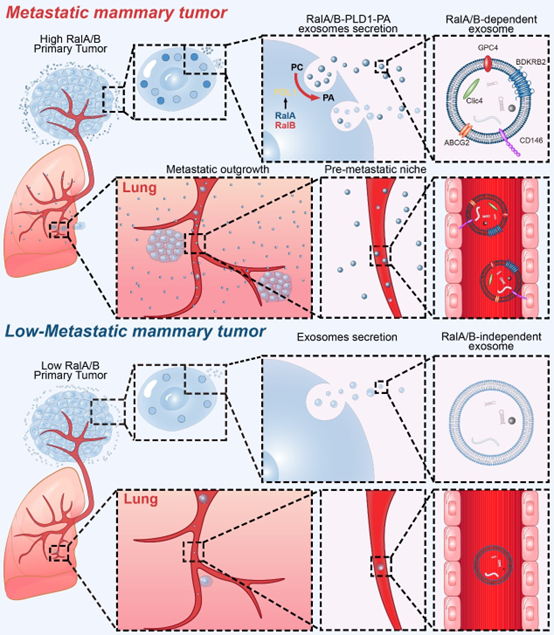
2、EVs通过调控免疫微环境和粘附分子促进乳腺癌肺转移前微环境的建立
接受化疗的乳腺癌细胞释放的evs中高水平的ptx3支持转移性乳腺癌细胞植入,并促进肺部中性粒细胞激活。同时,低let-7表达的evs通过lin28b和pd-l1路径诱导n2型中性粒细胞极化和t细胞抑制,而高Rala/b表达的乳腺癌细胞释放的evs通过外泌体cd146与肺血管内皮细胞结合,加速肺转移前微环境的建立,为肿瘤细胞的肺部植入铺路。
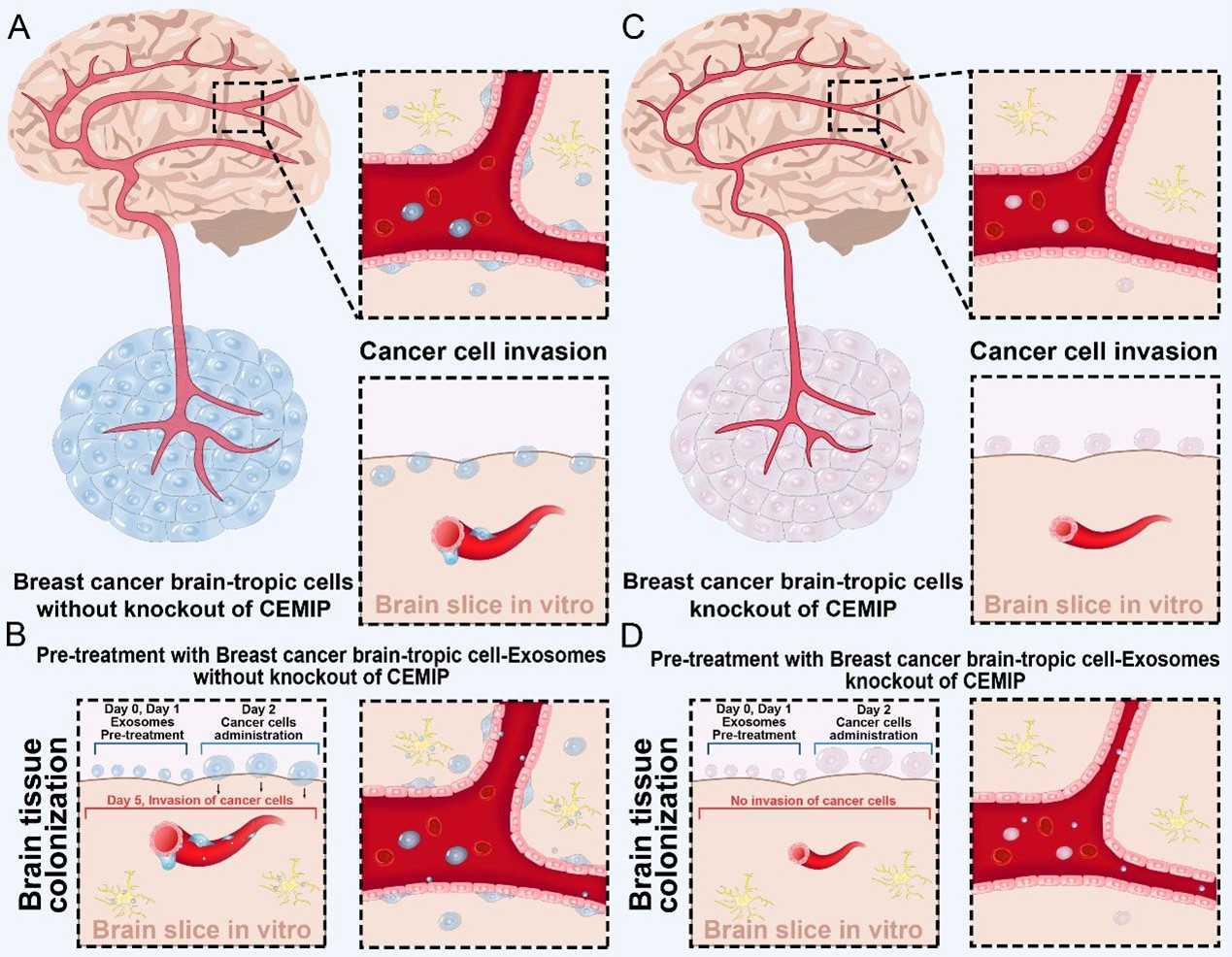
3、EVs通过破坏血脑屏障和诱导血管重塑促进乳腺癌脑转移前微环境的形成
使用来自乳腺癌细胞的EVs,通过携带的mir-181c,能够引起血脑屏障紧密连接蛋白的错位,进而破坏血脑屏障。而富含cemip的乳腺癌外泌体被小鼠脑内皮细胞和小胶质细胞摄取后,能够上调多种细胞因子,并促进脑血管重塑,从而促进乳腺癌细胞在脑内的入侵和植,促进乳腺癌细胞在脑内的转移,增加脑转移。
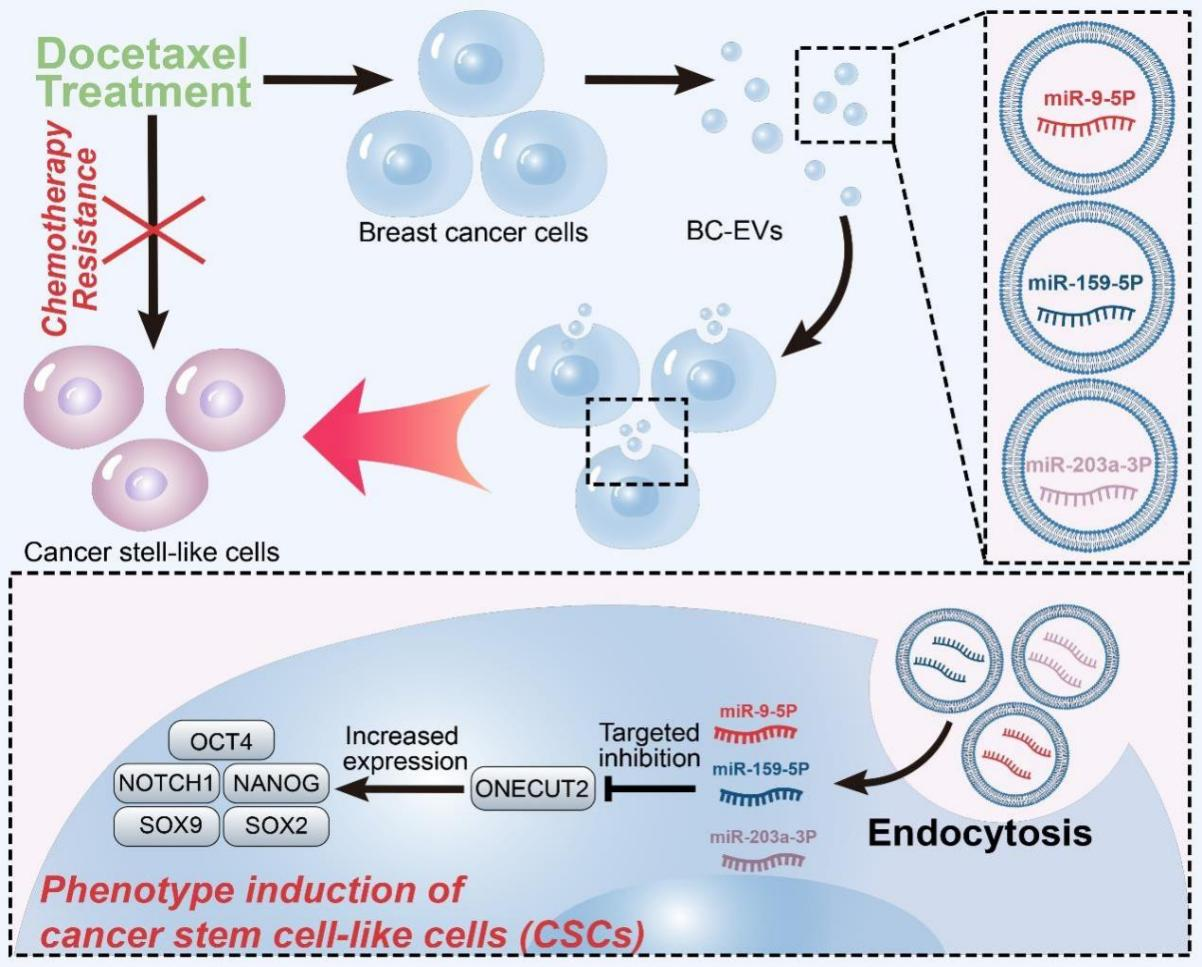
4、细胞外囊泡促进乳腺癌细胞的耐药性发展
耐曲妥珠单抗的her2+乳腺癌细胞释放出富含mir-567的外泌体,通过抑制atg5表达,从而阻止自噬,降低对曲妥珠单抗的敏感性。同时,化疗药物(多西他赛和吉西他滨)处理后的乳腺癌细胞释放的EVs携带mir-9-5p、mir-159-5p、mir-203a-3p等mirna和annexina6,能够抑制接受者细胞中肿瘤抑制基因的表达或降低egfr的泛素化和降解,从而将耐药性传递给敏感细胞。
5、细胞外囊泡通过重塑代谢和促进血管生成支持乳腺癌进展
乳腺癌EVs包含mir-122,靶向胰腺β细胞中的丙酮酸激酶以封装胰岛素生产和葡萄糖稳态,促进肿瘤生长。乳腺癌细胞摄取由肿瘤相关巨噬细胞释放的hisla-lncrna后,促进乳腺肿瘤细胞有氧糖酵解,因为hisla-lncrna被内化后抑制了hif-1α降解。此外,EVs通过各种分子,如携带的mir-182-5p,ev-epha2,circrna-hipk3和exo-anxa2,促进内皮细胞增殖,迁移和血管生成,为肿瘤生长提供营养并提供扩散途径。
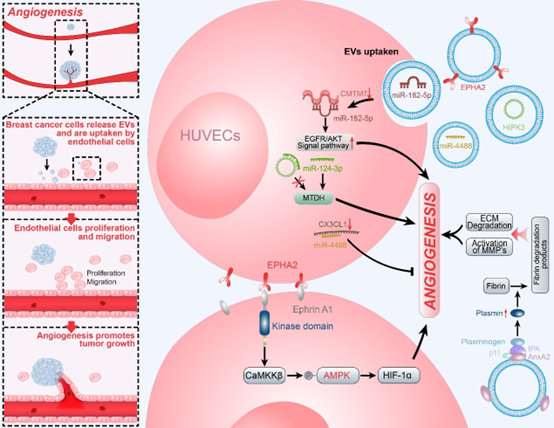
该综述揭示了EVs在乳腺癌转移和治疗抵抗中的关键作用,为理解肿瘤微环境的复杂调控提供了新视角;提出了EVs作为新型药物载体的可能性,为开发更精准、高效的乳腺癌治疗方案奠定了基础。未来,基于EVs的精准治疗策略可能成为乳腺癌治疗的新方向,帮助改善患者的生存率和生活质量。这项研究不仅深化了对乳腺癌发病机制的理解,也为其他癌症的研究提供了重要参考。
参考文献:
Extracellular vesicles: the “Trojan Horse” within breast cancer host microenvironments. Molecular Cancer, 2025, 24(1): 1-23.
外泌体资讯网 Molecular Cancer|辽宁省肿瘤医院康悦教授团队破解肿瘤微环境中"特洛伊囊泡"重塑乳腺癌转移路径