尽管已经实施了多种抗生素治疗方案治疗细菌性肺炎,但现有抗感染策略对细胞内细菌的疗效仍不理想。此外,抗生素治疗期间伴随的细胞因子风暴加剧了肺组织损伤。
近日,苏州大学附属第一医院 嵇富海、陈军、王旭、周好 / 南京邮电大学 丁显光团队在在国际权威期刊Biomaterials Research上发表题为“Molecular Targeting of Intracellular Bacteria by Homotypic Recognizing Nanovesicles for Infected Pneumonia Treatment”的学术研究论文(2025;29:172),报道了一种利用 M2型巨噬细胞衍生囊泡 [外泌体 (Exos)] 作为靶向递送抗生素 (Antibiotics@Exos)的载体,用于优化细菌性肺炎的治疗策略。
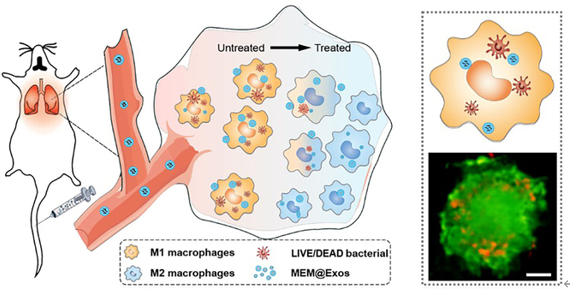
受最近关于 Exos 治疗炎症性疾病的研究的启发,该研究团队开发了一种改善重症肺炎治疗的感染靶向系统。将抗生素美罗培南(Meropenem,MEM) 与M2-Exos 一起加载以形成 MEM@Exos用于治疗细菌性肺炎。与肺炎治疗中用于加载抗生素的传统治疗方案相比,该技术代表了一项重大进步,可显著提高针对细胞内细菌的治疗结果并减轻炎症引起的肺组织损伤(图1),最终,改善了细菌性肺炎的治疗效果。
图 1. Antibiotics@Exos的靶向递送系统用于优化细菌性肺炎的治疗策略
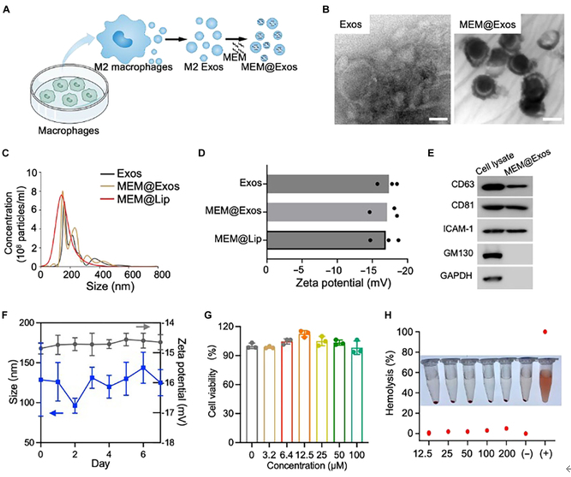
MEM@Exos的制备及表征(图2) 研究团队利用电穿孔策略将MEM加载到 M2-Exos 中以形成 MEM@Exos。在电穿孔处理后计算出 MEM 的相应负载效率为 2.2%,高于孵育法,与挤出法相当。透射电子显微镜、纳米粒径分析、Zeta 电位和Western blot等表征结果表明负载MEM后对M2-Exos 表面的结构及功能没有产生任何显著的影响。此外,溶血试验及CCK-8实验显示了MEM@Exos的生物安全性。
图2. MEM@Exos的制备及表征
MEM@Exos的炎症靶向性(图3) 为了确定 M2-Exos 对感染识别的炎性趋化性能力,初步研究的重点是评估它们靶向炎性M1型巨噬细胞的能力。正如“炎症趋化性理论”和“免疫亲和捕获理论”所证描述,M2-Exos具有良好的同源靶向性和高免疫亲和力。该研究结果表明,M2-Exos 可以靶向炎症部位并被炎症巨噬细胞有效内化,从而增强其靶向炎症反应的药物递送能力,表明 MEM@Exos 具有出色的生物相容性。同时,体内成像技术显示MEM@Exos可与炎症部位发生良好的共定位,从而有效解决了现有 Exos 靶向性差的问题,并且,它们表现出在肺炎部位保留时间长而不被清除的特征。
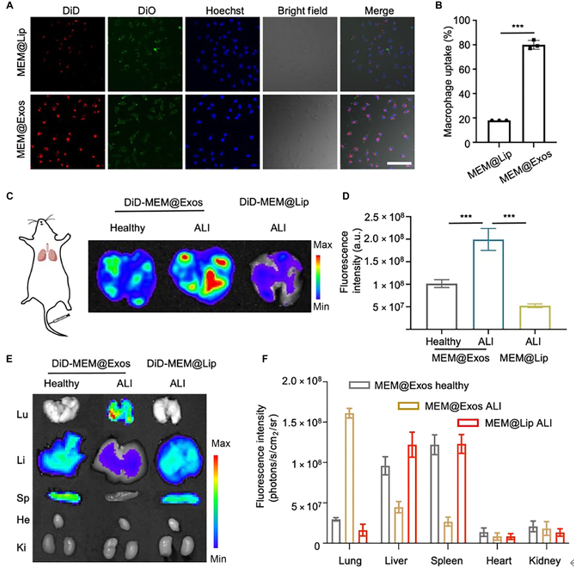
图3 MEM@Exos 的炎症靶向性
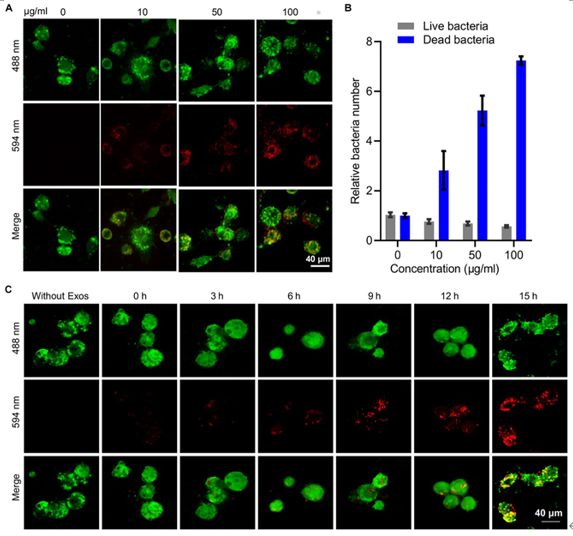
MEM@Exos的细胞内杀菌作用(图4) M2-Exos与其亲本巨噬细胞具有良好的组织相容性,这促进了 MEM 转运到细胞中。M2-Exos 中的 MEM 可以有效杀伤被巨噬细胞吞噬后的活大肠杆菌。此外,随着 MEM@Exos 浓度的增加和时间的延长,细胞内杀菌作用逐渐增强。这些发现最终证明 M2-Exos 能够有效地将外源性抗生素转运到炎性M1型巨噬细胞中,有助于完成细胞内灭菌。这种能力归因于M2-Exos出色的组织相容性。
图4 MEM@Exos 的细胞内杀菌作用
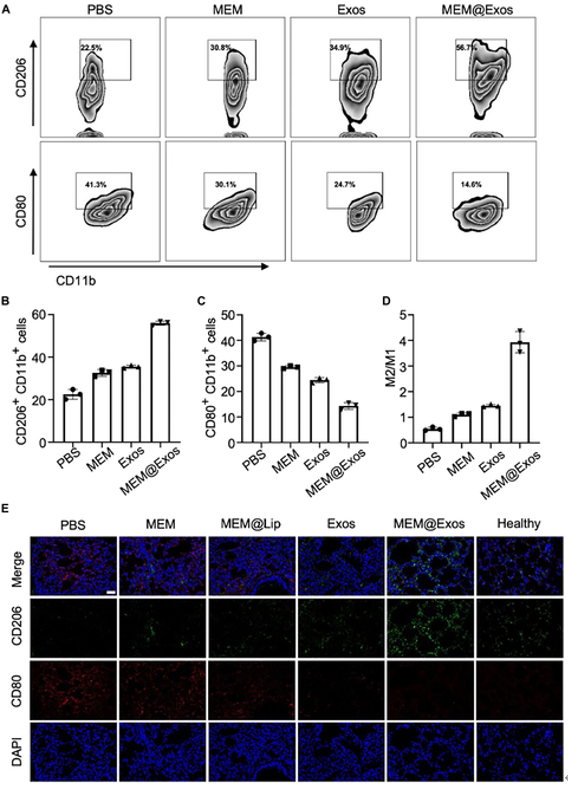
MEM@Exos可将炎性M1型巨噬细胞重编程为抗炎 M2 型(图5) M2-Exos具有良好的免疫调节功能,可以将单核细胞重编程为 M2 型极化。同时,M2-Exos 中包裹的 MEM 可以杀死大肠杆菌,导致内源性 LPS 减少,有助于削弱 M1 型的极化程度。流式细胞术和肺组织的免疫荧光染色技术结果表明MEM@Exos纳米复合材料能够将巨噬细胞重新编程为 抗炎M2型极化,从而促进抗炎微环境的产生。这样的环境有利于缓解与炎性 M1型巨噬细胞相关的强大“细胞因子风暴”,这对缓解ALI具有非常重要的意义。
图5 MEM@Exos将炎性M1型巨噬细胞重编程为抗炎 M2 型
MEM@Exos 改善 ALI 小鼠的炎症反应(图6) 在该研究中,ALI小鼠肺组织中浸润的白细胞数量显著减少,并且炎症因子 TNF-α 分泌显著减少,抗炎因子 IL-10 升高。随着时间的推移,最初的炎症环境逐渐转变为抗炎微环境。此外,体内动物实验结果表明,MEM@Exos可以减轻炎性细胞因子风暴,缓解肺泡水肿,减少 ROS 损伤,并最终治疗重症肺炎。更重要的是,它对主要器官没有明显的毒副作用。
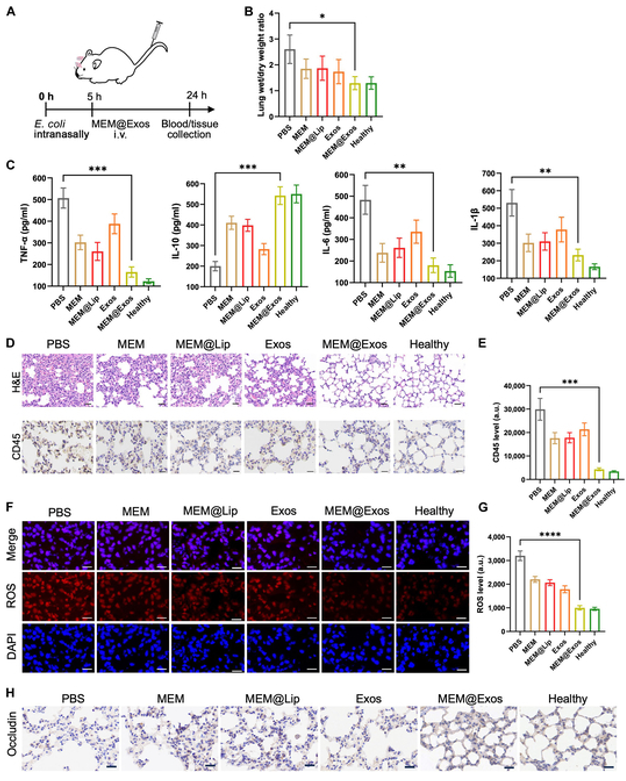
图6 MEM@Exos 改善 ALI 小鼠的炎症反应
该研究成功开发了一种感染靶向平台(Antibiotics@Exos),用于细胞内杀菌和细菌性肺炎的治疗。开发的MEM@Exos不仅可靶向细菌感染部位,还可抑制炎症因子的产生,并通过将巨噬细胞重编程为M2 型表型来缓解炎症应激反应。值得注意的是,M2-Exos 可作为保护性“盔甲”,将抗生素递送至炎性巨噬细胞中,从而增强抗生素的渗透性,解决细胞内细菌感染。该团队开发的这种生物活性平台具有重要的应用前景,可作为治疗严重传染性疾病的新型治疗策略。
苏州大学附属第一医院嵇富海教授、陈军教授和南京邮电大学丁显光教授是论文的共同通讯作者。苏州大学附属第一医院王旭、周好是论文的共同第一作者。
参考文献:
Molecular Targeting of Intracellular Bacteria by Homotypic Recognizing Nanovesicles for Infected Pneumonia Treatment. Biomater Res. 2025; 29: 172.
外泌体资讯网 Biomater Res|苏大附一院嵇富海/陈军/王旭/周好/南京邮电大学丁显光:通过同源识别纳米囊泡靶向细胞内细菌治疗肺部感染