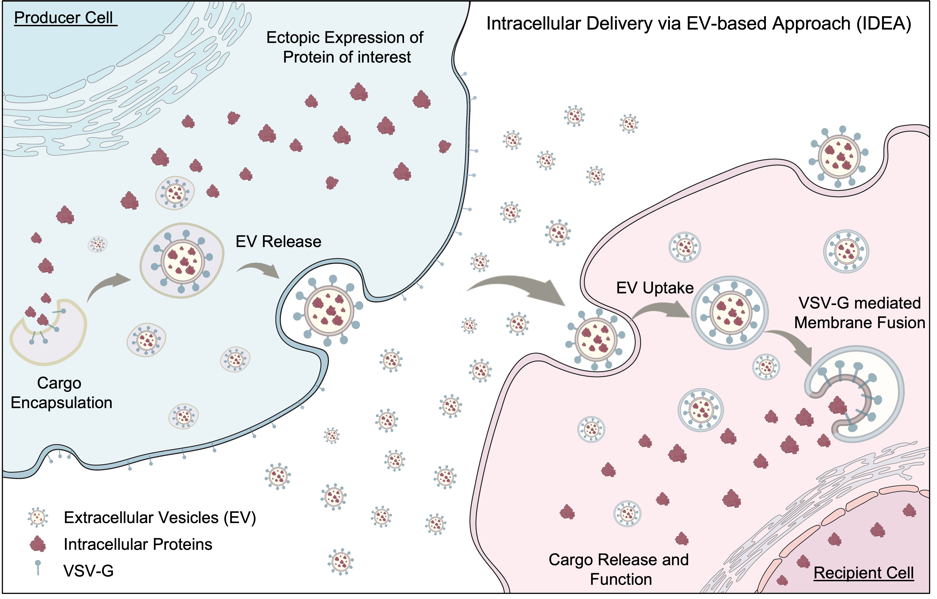
蛋白质作为生命活动的主要生物大分子,在药物研发中展现出独特的优势。相较于小分子药物,蛋白质药物具有更高的特异性和更低的毒副作用;相比于基因治疗,蛋白质药物不会引起永久性的遗传改变,因此备受瞩目。由于蛋白质自身的独特属性,如大尺寸、亲水性、膜不通透性和易降解等特点,目前临床批准的蛋白质药物靶点仅限于胞外环境中的配体或细胞表面分子,然而,人类大部分蛋白质属于胞内蛋白。目前胞内蛋白递送通常依赖于阳离子脂质体、聚合物、无机纳米材料等蛋白包封载体,或近年来兴起的通过工程化细菌或类病毒颗粒VLP传递,但以上策略往往需要对蛋白质进行修饰,也存在蛋白质装载和溶酶体逃逸效率低、免疫原性高等缺点。如何实现高效的胞内蛋白递送仍是该领域一大挑战。近日,中国科学技术大学生命科学与医学部程临钊/刘森泉/马丁团队于Protein & Cell杂志在线发表题为Engineered extracellular vesicles enable high-efficient delivery of intracellular therapeutic proteins的研究性论文(2024 Mar 22:pwae015)。报道了一种新型高效的胞内蛋白递送策略,称为Intracellular delivery via EV-mediated Approach(IDEA),该策略利用细胞外囊泡(Extracellular Vesicles,EVs)作为载体,成功将胞内蛋白递送到细胞质或细胞核内实现其生物功能。这一策略克服了传统EVs载荷富集方法中必须使用融合支架的局限性,实现了对多种天然胞内蛋白的高效装载及递送,为蛋白质药物的研发和应用开辟了新的道路。
细胞外囊泡是一类由细胞主动分泌的具有双层膜结构的天然纳米级颗粒。EVs凭借良好的结构稳定性,并具备较好的生物相容性、低免疫原性以及保护内容物不被降解和跨越生理障碍等方面的优势,近年来已成为有效递送生物活性物质的新兴载体4。首先该研究详细探讨了IDEA平台的工作机制和优势。通过一种基于Cre-loxP重组的体内外报告系统,研究人员证实了工程化EVs能够成功递送Cre重组酶至靶细胞核内,从而高效激活DNA重组。此外,作者通过多个不同肿瘤模型初步证实IDEA在肿瘤免疫治疗中的巨大潜力。通过利用细胞外囊泡作为载体,研究人员成功地实现了生物活性蛋白的高效传递,为基因和蛋白治疗领域带来了新的希望。这项研究开发的基于工程化细胞外囊泡的胞内蛋白高效递送平台弥补了以往蛋白递送工具的不足,为蛋白质治疗领域带来了全新的发展机遇,为开发更多有效的细胞内治疗策略提供了新的思路和技术支持。未来,研究人员将对其进一步优化,以拓展其在不同疾病治疗中的应用。课题组除了研究天然外泌体的功能性质外(Stem Cells. 2019, DOI: 10.1002/stem.2996; Journal of Extracellular Vesicles. 2021, DOI: 10.1002/jev2.12054),还对外泌体作为蛋白递送平台用于疾病治疗进行了探索,结合课题组之前开发的基于细胞外囊泡的分泌蛋白和膜蛋白递送系统(Advanced Science. 2023, DOI: 10.1002/advs.202206606),将为疾病治疗提供更加可靠和有效的解决方案,以期在生物医学领域取得新突破。Engineered extracellular vesicles enable high-efficient delivery of intracellular therapeutic proteins, Protein Cell. 2024 Mar 22:pwae015. doi: 10.1093/procel/pwae015. 外泌体资讯网 Protein & Cell|中国科大刘森泉/马丁团队:一种新型高效的胞内蛋白递送策略