外泌体的大小范围为50-150纳米,是不同细胞之间相互联系的媒介,逐渐在药物输送、诊断、免疫疗法和精准医疗领域发挥越来越重要的作用。为了提高治疗效率并降低纳米材料的毒性,越来越多的科研工作者聚焦于探索纳米材料改造外泌体的研究。然而,目前的方法(如超声或电穿孔)难免破坏外泌体膜和其中的生物活性分子,其临床应用受到限制。近日,上海长海医院宋洪元/沈炜、南京大学医学院顾宁联合在ACS Nano上发表了题为“Iron Oxide Nanoparticles Engineered Macrophage-Derived Exosomes for Targeted Pathological Angiogenesis Therapy”的研究论文(doi: 10.1021/acsnano.4c00699),提出了细胞生物反应器辅助纳米材料修饰外泌体的概念。文章的第一作者为张昊瑞,毛宇和聂政;通讯作者为顾宁,沈炜和宋洪元。
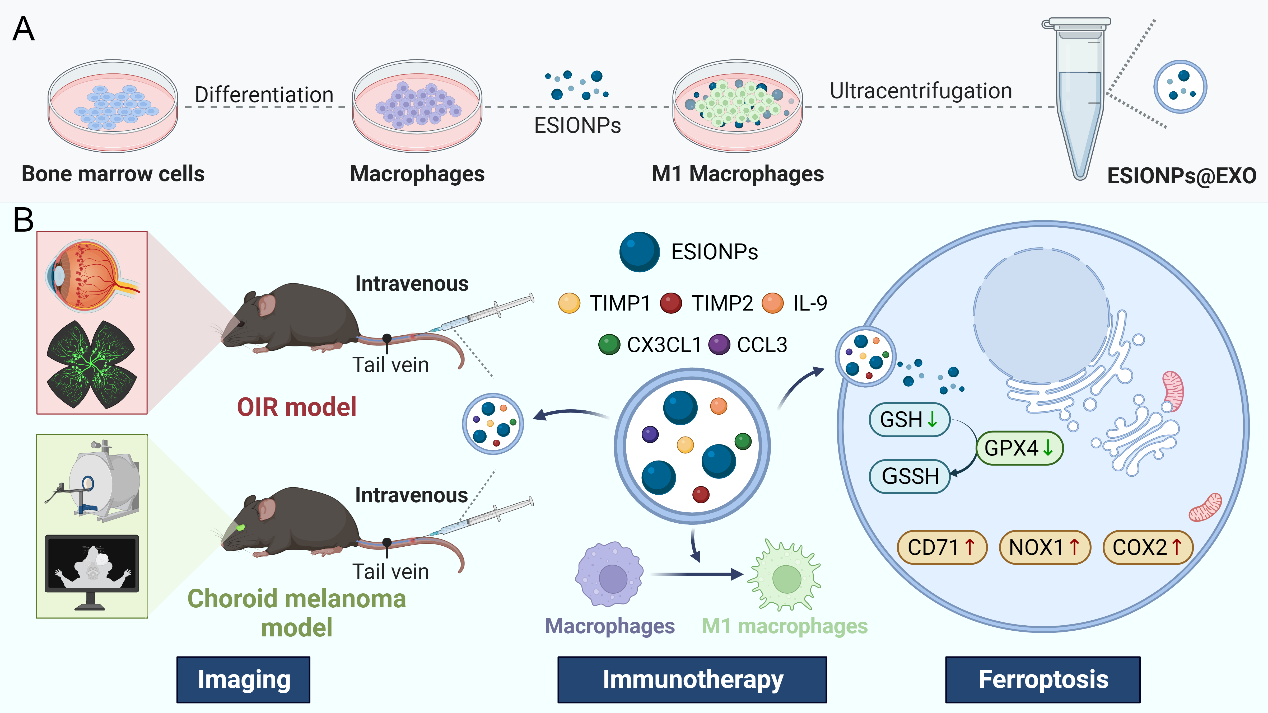
这项究将巨噬细胞作为生物反应器,分离制备了包含氧化铁纳米颗粒的外泌体,该外泌体同时具备增强磁共振成像效果、诱导铁死亡反应和靶向治疗病理性新生血管的特性。通过对极小尺寸氧化铁纳米颗粒 ( ESIONPs) 诱导的 M1 极化巨噬细胞分泌的外泌体进行分选,获得了包裹ESIONPs的 外泌体(ESIONPs@EXO) 。ESIONPs@EXO 可抑制体内外病理性新生血管,且在治疗剂量下无明显毒性。此外,ESIONPs@EXO 还能靶向病理性新生血管部位,并在磁共振成像中表现出优异的 T1 加权对比特性。ESIONPs@EXO可诱导铁死亡对病理性新生血管进行免疫治疗。这些研究结果表明,利用巨噬细胞以纯生物方法设计的 ESIONPs@EXO 具有靶向治疗病理性新生血管的潜力。图1. ESIONPs@EXO 制备(A)和靶向治疗病理性新生血管(B)示意图该研究可以为病理性新生血管的治疗提供一种新的治疗选择,并具有临床转化的潜力。Iron Oxide Nanoparticles Engineered Macrophage-Derived Exosomes for Targeted Pathological Angiogenesis Therapy, ACS Nano.2024 Feb 27. doi: 10.1021/acsnano.4c00699.外泌体资讯网 ACS Nano | 上海长海医院宋洪元/沈炜、南京大学医学院顾宁:工程化巨噬细胞外泌体为病理性新生血管治疗提供新思路