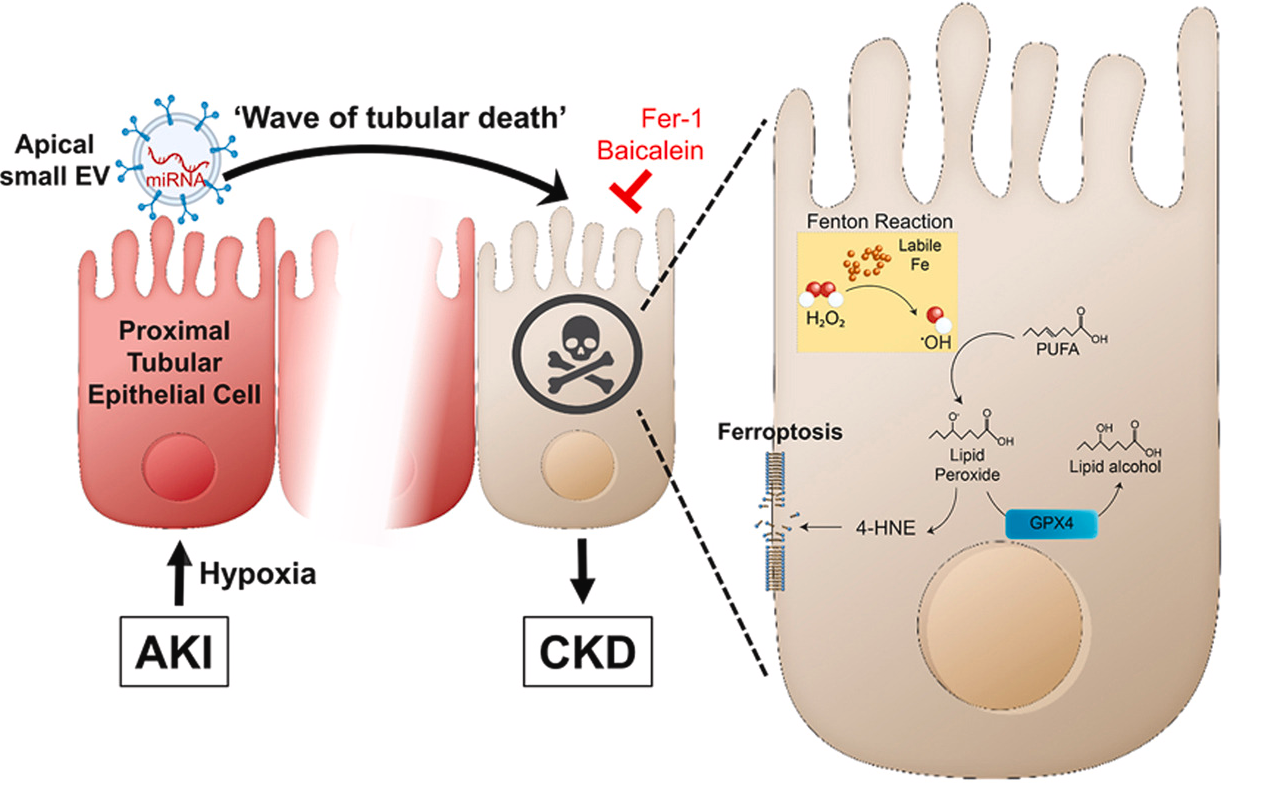
缺氧是导致肾小管氧化应激和细胞死亡的关键病理生物触发因素,推动了急性肾损伤(AKI)向慢性肾脏病(CKD)的过渡。富含线粒体的近端肾小管上皮细胞(PTEC)对缺氧非常敏感,在推动AKI到CKD过渡的持续肾小管丧失中起着关键作用。
近日,来自澳大利亚皇家布里斯班妇女医院的研究人员揭示了PTEC来源的小细胞外囊泡(sEV)在传播“肾小管死亡浪潮”中的作用。他们发现,在缺氧条件下,来自顶端PTEC膜(而非基底端膜)的sEV产量显著增加,缺氧顶端sEV具有独特的“促伤害”miRNA特征,并在同源PTEC中触发脂质过氧化和铁死亡的“肾小管死亡浪潮”。该研究首次提供了在AKI到CKD过渡中的概念的原位证据。相关内容以“Human proximal tubular epithelial cell-derived small extracellular vesicles mediate synchronized tubular ferroptosis in hypoxic kidney injury”为题在线发表于1月14日的国际知名氧化还原生物学领域学术期刊Redox Biology上。
急性肾损伤(AKI)是一个严重的公共卫生问题,全球每年发病超过1300万人次。AKI是慢性肾病(CKD)发展和进展的危险因素,与无AKI的住院患者相比,AKI幸存者患CKD的风险增加了8.8倍。肾小管间质缺氧是AKI到CKD过渡的一个标志性特征。严重AKI情况下,周围肾小管毛细血管稀疏和血流减少,形成局部的肾小管间质缺氧微环境,触发小管上皮细胞(TEC)氧化应激和死亡途径,最终导致肾小管间质纤维化和CKD的发展。阐明这种缺氧肾小管细胞枯竭的复杂分子信号机制对于开发精准治疗,以干预AKI到CKD的过渡,是至关重要的。
近端肾小管上皮细胞(Proximal tubular epithelial cells,PTEC)在驱动AKI到CKD过渡中发挥着中心作用。PTEC的高能量需求主要由线粒体脂肪酸氧化提供,这是一个氧气密集型的过程。因此,在严重AKI后,PTEC对缺氧损伤特别脆弱。人PTEC在缺氧条件下经历氧化应激和铁死亡,这是一种铁依赖性的坏死形式,由以下因素触发:(1)铁死亡激活剂和金标准生物标志物酰基辅酶A合酶长链家族成员4(ACSL4);(2)脂质修复酶谷胱甘肽过氧化物酶4(GPX4)的减少表达;(3)有毒脂质过氧化物(最终产物4-羟基壬烯醛;4-HNE)的积累。此前研究发现,缺氧AKI损伤通过一种同步铁死亡的机制沿着小鼠近端肾小管传播,触发相邻细胞中进行性的肾小管细胞死亡。然而,尚未定义PTEC衍生的死亡信号是如何传播这种铁死亡的“肾小管死亡浪潮”的。
小细胞外囊泡(sEV)是细胞间信号传递的基本组成部分。sEV根据其尺寸分布(50-150 nm直径)和表达标准的sEV蛋白(如CD9)、ESCRT系统蛋白(如肿瘤易感基因TSG101)的组分以及热休克蛋白(如HSP70、HSP84)来定义。sEV通过将其包含的分子货物(如miRNA)从母细胞转移到受体细胞来在细胞之间传递信号。先前研究显示,在缺氧条件下,人PTEC分泌数量增加的sEV(在早期的出版物中一般称为外泌体),具有独特的分子(miRNA、蛋白质)细胞死亡信号。然而,PTEC是极化的上皮细胞,它们顶端膜的细胞外环境与其底部膜的环境不同(即肾小管腔/尿液空间与肾小管间质)。研究已经表征了PTEC对有害刺激的极性依赖性反应(如表面分子和细胞因子在顶端与基底膜的表达)。此前研究还证明了在炎症性疾病条件下,人PTEC释放的sEV是具有极性的。
在这项研究中,研究人员试图探讨患者来源的PTEC在AKI到CKD过渡的缺氧条件下释放的sEV在极性依赖性上的数量和载货差异。研究人员通过体外培养患者来源的PTEC,在Transwell插片上在常氧(21% O2)和低氧(1% O2)条件下,分离和分析从顶侧和基底侧PTEC表面分泌的sEV。与常氧PTEC相比,缺氧PTEC的顶侧表面分泌的sEV数量增加。在培养条件之间未观察到基底侧sEV数量的差异。对缺氧顶侧sEV货物的生物学通路分析确定了与细胞损伤通路相关的不同miRNA。在功能实验中,与常氧顶侧sEV相比,缺氧顶侧sEV选择性地诱导同源PTEC的铁死亡(谷胱甘肽过氧化物酶-4下调,脂质过氧化上调) 。铁死亡抑制剂ferrostatin-1和baicalein的添加减轻了PTEC的铁死亡。对缺氧顶侧sEV进行RNA酶A预处理抵消了PTEC的铁死亡,证明了sEV RNA在铁死亡“死亡浪潮”信号中的作用。与这些体外发现一致,对具有AKI进展为CKD的患者进行的诊断性肾活检的原位免疫标记显示存在铁死亡的传播迹象(表现为增加的ACSL4 PTEC),而来自这些“AKI到CKD过渡”患者的尿源sEV(usEV)在功能研究中触发了PTEC的铁死亡(脂质过氧化上调)。
这项研究的数据确定了PTEC来源的顶侧sEV及其囊内RNA作为缺氧肾损伤中肾小管脂质过氧化和铁死亡的介质。这种肾小管从初始损伤传播到“死亡浪潮”的机制,提供了新的治疗检查点,用于针对AKI到CKD过渡患者。
参考文献:Human proximal tubular epithelial cell-derived small extracellular vesicles mediate synchronized tubular ferroptosis in hypoxic kidney injury. Redox Biol 2024. Doi:10.1016/j.redox.2024.103042.