腹膜转移是胃癌最常见的转移方式,由于其发病率高、生存期短,是胃癌晚期高死亡率的主要原因之一。当前胃癌腹膜转移的临床诊断仍依赖于影像学检查和侵入性的腹腔镜探查,诊断结果常滞后于病情。因此,提高对隐匿性胃癌腹膜转移的早期诊断和筛查对提高患者生存率具有重要意义。目前,针对癌症相关生物标志物的液体活检逐渐成为癌症诊断和动态监测的重要的诊疗指标。外泌体大量存在于各种体液中,携带蛋白,核酸,脂质等生物分子介导癌细胞与正常细胞间通讯,影响肿瘤进展和转移。随胃癌进展所产生的腹水中外泌体能够作为液体活检的主要生物标志物,辅助进行胃癌腹膜转移早期诊断。电化学发光(ECL)分析方法针对外泌体检测具有灵敏度高、响应速度快等优势。结合具有高光场约束和电磁场增强能力的等离子体纳米腔结构构建电化学发光传感体系,能够提高分析灵敏度和分辨能力,为外泌体的检测和疾病临床诊断提供新的策略。
近日,吉林大学化学学院马强教授团队开发了基于等离子体纳米腔结构的电化学发光传感器用于检测腹水外泌体中的miRNA并对胃癌腹膜转移情况进行了评估。相关成果以“Plasmonic nanocavity-modulated electrochemiluminescence sensor for gastric cancer exosomal miRNA detection”为题发表在Biosens Bioelectron上(DOI: 10.1016/j.bios.2023.115847)。
图1. 基于等离子体纳米腔结构的ECL传感器对腹水外泌体miRNA检测示意图
这一研究工作中,以硫点作为ECL纳米发光探针,通过金纳米片自组装薄膜、DNA四面体结构以及金纳米粒子构建了具有高度光场局域能力和电磁场增强的等离子体纳米腔以调控光学局域态密度,产生强ECL信号。同时,金纳米粒子作为光学纳米天线使ECL转变为定向的偏振发射,提高了ECL传感体系的灵敏度和分辨能力。因此,基于等离子体纳米腔调制的电化学发光传感器在1 fM-1 nM线性范围内实现了对miRNA-223-3p的灵敏检测,检测限为0.14 fM。外泌体中miRNA-223-3p的高表达会促进胃癌的侵袭和腹膜转移,能够作为胃癌腹膜转移情况识别和诊断的标志物及评价指标。因此,对胃癌患者腹水外泌体中miRNA-223-3p的表达水平进行了检测。结合临床诊断信息分析,ECL检测结果显示胃癌晚期(III/IV)外泌体miRNA水平高于胃癌早期(I/II)。同时,在脱落细胞学检查和胃癌腹膜转移临床诊断中呈阳性结果的样本显示出外泌体miRNA高度表达。结果表明,该工作建立的ECL传感器实现了对于外泌体miRNA-223-3p的灵敏检测,能够评估胃癌分期,具有辅助胃癌腹膜转移早期诊断的应用潜力。
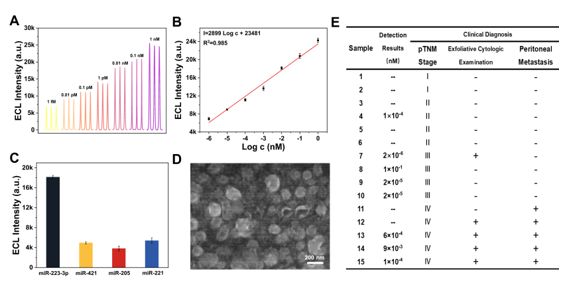
图2. ECL传感器对miRNA-223-3p的检测性能及对胃癌患者腹水样本的分析结果。
吉林大学化学学院博士研究生王培琳是本论文的第一作者,吉林大学化学学院马强教授是论文的通讯作者,本文得到了国家自然科学基金和吉林省科技发展计划项目的支持。
参考文献:
Plasmonic nanocavity-modulated electrochemiluminescence sensor for gastric cancer exosomal miRNA detection. Biosensors and Bioelectronics 245 (2024) 115847. DOI: 10.1016/j.bios.2023.115847.
外泌体资讯网 Biosens Bioelectron |吉林大学马强:基于等离子体纳米腔调制的电化学发光传感器对腹水外泌体miRNA的检测研究