重症肌无力(MG)是一种由神经-肌肉接头传递功能障碍引起的、罕见的慢性自身免疫性神经肌肉疾病,由于MG病程长、难治疗、多复发,故而寻找新型生物制剂具有重要临床意义。近日,山东第一医科大学第一附属医院段瑞生教授团队在Journal of controlled release(JCR Q1 IF:10.8)发表了题为 “Extracellular vesicles encapsulated with caspase-1 inhibitor ameliorate experimental autoimmune myasthenia gravis through targeting macrophages ”的研究论文(2023 Nov 8:364:458-472),首次报道了负载Caspase-1抑制剂的树突状细胞来源细胞外囊泡在重症肌无力中的治疗作用及机制,具有很高的临床转化潜力。 第一作者为山东第一医科大学第一附属医院博士研究生周阳、神经内科杜通医师,通讯作者为神经内科学术带头人段瑞生教授、王聪聪副教授。
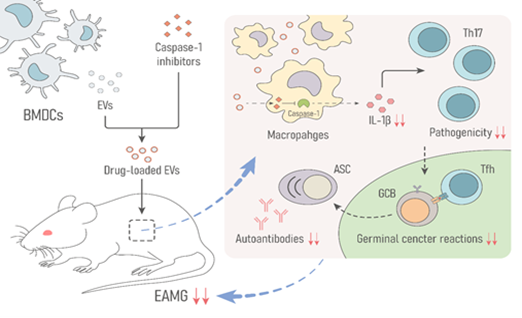
作者前期研究已证实炎症小体中的半胱氨酸天冬氨酸酶(Caspase-1)在MG患者急性期及实验性自身免疫性重症肌无力(EAMG)大鼠中表达明显升高,可作为治疗MG新靶点,进一步证实应用Caspase-1 抑制剂可以明显缓解EAMG大鼠的临床症状和减少致病性抗体生成。然而,长期应用Caspase-1 抑制剂因其组织毒副作用、无细胞靶向性限制了临床应用。这项研究证实负载Caspase-1抑制剂的树突状细胞来源细胞外囊泡(DC-EVs)在体内天然靶向组织巨噬细胞发挥治疗作用,通过降低IL-1β,抑制致病性Th17,抑制生发中心反应,从而降低致病性抗体水平,最终达到缓解疾病进展的目的。更重要的是,负载Caspase-1抑制剂的DC-EVs显示比常规药物剂量更好的治疗效果,并显著减少组织毒性,最终达到“剂半功倍”“一箭双雕”的效果。这项研究表明EVs作为一种新型药物输送载体在生物治疗与临床转化方面具有巨大潜力,通过负载Caspase-1抑制剂的EVs在重症肌无力等自身免疫性疾病治疗中具有良好临床应用前景。Extracellular vesicles encapsulated with caspase-1 inhibitor ameliorate experimental autoimmune myasthenia gravis through targeting macrophages, J Control Release. 2023 Nov 8:364:458-472. doi: 10.1016/j.jconrel.2023.11.006.外泌体资讯网 J Control Release | 山东第一医科大学第一附属医院段瑞生团队:树突状细胞来源的细胞外囊泡治疗重症肌无力新策略