内皮细胞(EC)上的CD36控制了组织脂肪酸(FA)摄取。来自美国华盛顿大学医学院的研究人员对ECs如何转移FAs进行了研究,发现FA与CD36的相互作用可诱导小窝蛋白-1的第14位酪氨酸(Cav-1 Y14)被Src激酶的磷酸化和神经酰胺的生成,随后裂变产生含有FA、CD36和神经酰胺的囊泡,这些囊泡以小外泌体样细胞外囊泡(sEV)的形式在基底侧分泌,抑制小鼠的该sEV通路可减少肌纤维对FA的摄取并可增加循环FA水平。相关研究以“Endothelial cell CD36 regulates membrane ceramide formation, exosome fatty acid transfer and circulating fatty acid levels”为题在线发表于7月7日的国际知名学术期刊、Nature子刊Nature Communications杂志上。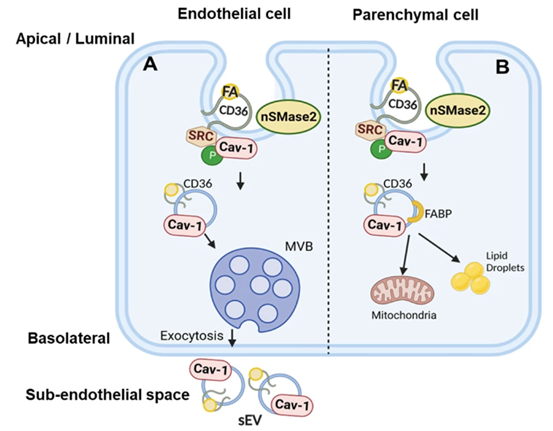
长链脂肪酸(fatty acids,FAs)在细胞膜结构和功能中起着重要作用,它们在全身能量代谢中至关重要,而且线粒体FA氧化是心脏和肌肉的有效ATP来源,FA酯化成甘油三酯为脂肪和其他组织提供能量储存能力。脂肪酸氧化也影响干细胞的健康和组织更新。在能量代谢的生理转变过程中,细胞FA摄取和利用的波动对于维持体内平衡至关重要,因为循环中的FA被输送到特定组织。在禁食或运动时,当葡萄糖供应减少时,脂肪组织脂肪酶从储存的甘油三酯(TG)中动员FAs,以增加循环FAs的供应。同时,心脏和肌肉组织上调FA的摄取和氧化,同时减少葡萄糖的利用,从而节省葡萄糖储备。相反,当进食使更多的葡萄糖可利用时,葡萄糖在心脏和肌肉中的使用量增加,更多的脂肪被直接储存在脂肪库中。 在组织中,FA摄取主要发生在毛细血管水平,FA通过微血管内皮细胞(microvascular endothelial cells,MECs)的转移而完成摄取流程。MEC上的表面高亲和力FA受体需要识别FAs,并与细胞内FA结合蛋白和FA酰基辅酶A连接酶协同工作,以促进快速脂质积累。在血液循环中,脂肪酸与白蛋白结合或在脂蛋白甘油三酯中酯化。血管内脂蛋白脂肪酶(lipoprotein lipase,LpL)及其内皮细胞(EC)锚定蛋白Gpihbp1介导脂蛋白中FA的释放。LpL在EC表面释放的未酯化FA水平可能高于循环中从白蛋白解离的FA水平,但目前原因尚不清楚。 几种蛋白质影响细胞FA摄取,包括FA转运(FATP)家族成员、FA结合蛋白(FABPs)、酰基辅酶A合成酶和分化簇蛋白36 (CD36)。这些蛋白可以在不同水平的摄取过程中发挥作用,包括质膜转移或FA的细胞内通道。质膜糖蛋白CD36通过与油酸的一种反应性膜非渗透性磺基琥珀酰亚基衍生物SSO14的亲和标记,被鉴定为FA转运体,并在啮齿动物和人类中证实了其在组织FA摄取中的生理作用。除了白蛋白结合的循环FAs外,CD36还转移LpL从极低密度脂蛋白(VLDL)中释放的FAs,然而乳糜微粒水解对FA的摄取是不依赖CD36的。CD36的晶体结构及其家族成员(包括SR-B1和Limp2)揭示了一个共同的内部脂质运输通道,并且在CD36晶体的通道中发现了长链FAs。根据对晶体结构的模拟,FAs结合在CD36的疏水表面袋中,并连接到通道里。 CD36在毛细血管内皮中高度表达,它是决定微血管细胞脂质处理的基因表达标志的一部分。来自EC特异性缺失各种转录因子的有力证据支持内皮在组织FA摄取中的屏障功能,EC特异性缺失CD36的研究支持其在这一过程中的关键作用:内皮细胞缺乏CD36 (EC-Cd36−/−)的小鼠对脂肪组织、心脏、骨骼肌和胃粘膜的FA摄取受损。EC-Cd36−/−小鼠也表现出在种系Cd36−/−小鼠中观察到的更高的血浆FAs和增强的葡萄糖摄取能力。 在这项研究中,研究人员探讨了内皮细胞如何将外源性FA转移到实质细胞的机制。我们发现,FAs诱导CD36依赖性的小窝蛋白-1(caveolin-1,Cav-1)磷酸化,并在小窝中产生神经酰胺,这与小窝出芽形成含有FA、CD36、Cav-1和神经酰胺的内囊泡(IVs)有关。这些囊泡随后作为外泌体样的小细胞外囊泡(sEV)释放到基底外侧膜,将FAs运送到组织细胞。研究人员观察到sEV中的FAs在transwell中向底层肌纤维转移。在EC表达外泌体标记物emerald GFP-CD63的小鼠中,肌肉纤维在emGFP标记的点中积累循环FAs。FA-sEV通路会通过CD36缺失、阻断肌动蛋白重塑、Src抑制、Cav-1 Y14突变和中性鞘磷脂酶2抑制而抑制。抑制小鼠sEV的形成减少肌肉FA的摄取,增加循环FAs(仍留在血管中),降低葡萄糖,类似Cd36-/-小鼠表型。研究结果表明,FA摄取影响膜神经酰胺形成、内吞作用以及EC与实质细胞的通讯。 参考文献:Endothelial cell CD36 regulates membrane ceramide formation, exosome fatty acid transfer and circulating fatty acid levels. Nat Commun. 2023 Jul 7;14(1):4029.外泌体资讯网 NatCommun丨内皮细胞CD36调节脂肪酸的经外泌体转移和神经酰胺形成





