间充质干细胞是一种多能干细胞,具有强大的分化潜能,以及自我复制、支持造血、定向迁移、免疫调节、组织器官损伤修复的能力。越来越多的研究表明,间充质干细胞移植主要是通过旁分泌途径发挥作用,而不是通过细胞分化或融合途径拯救受损细胞。间充质干细胞分泌的外泌体显示出与其亲本细胞相似的治疗效果,基于外泌体的无细胞疗法以其天然的优势成为再生医学领域的一颗新星。与间充质干细胞相比,外泌体可以避免干细胞疗法潜在的风险,包括免疫反应和致瘤性,且更便于储存和运输。外泌体具有磷脂双分子层结构,是天然的生物分子载体,具有生物相容性,更具稳定性,其纳米级别的尺寸使其能够越过生物屏障。然而,外泌体的产量有限,难以满足潜在的临床需求,严重阻碍了其临床转化的进程。
近日,山东大学药学院王凤山、张新科团队在Life Sciences上发表了题为“Challenges and strategies: Scalable and efficient production of mesenchymal stem cells-derived exosomes for cell-free therapy”的综述 ( 2023 Feb 22;319:121524),针对间充质干细胞来源外泌体走向临床所面临的挑战,提出了相应解决方案和展望。文章概述了外泌体的生成机制,着重讨论了提高外泌体产量的方法,并介绍了间充质干细胞来源外泌体在组织器官损伤修复领域的应用。王凤山教授和张新科副教授为共同通讯作者,研究生潘威为第一作者,山东大学为第一完成单位和唯一通讯单位,山东省立医院、美国加州大学戴维斯分校作为论文参与单位。该工作得到了国家自然科学基金和山东省自然科学基金等项目的支持。
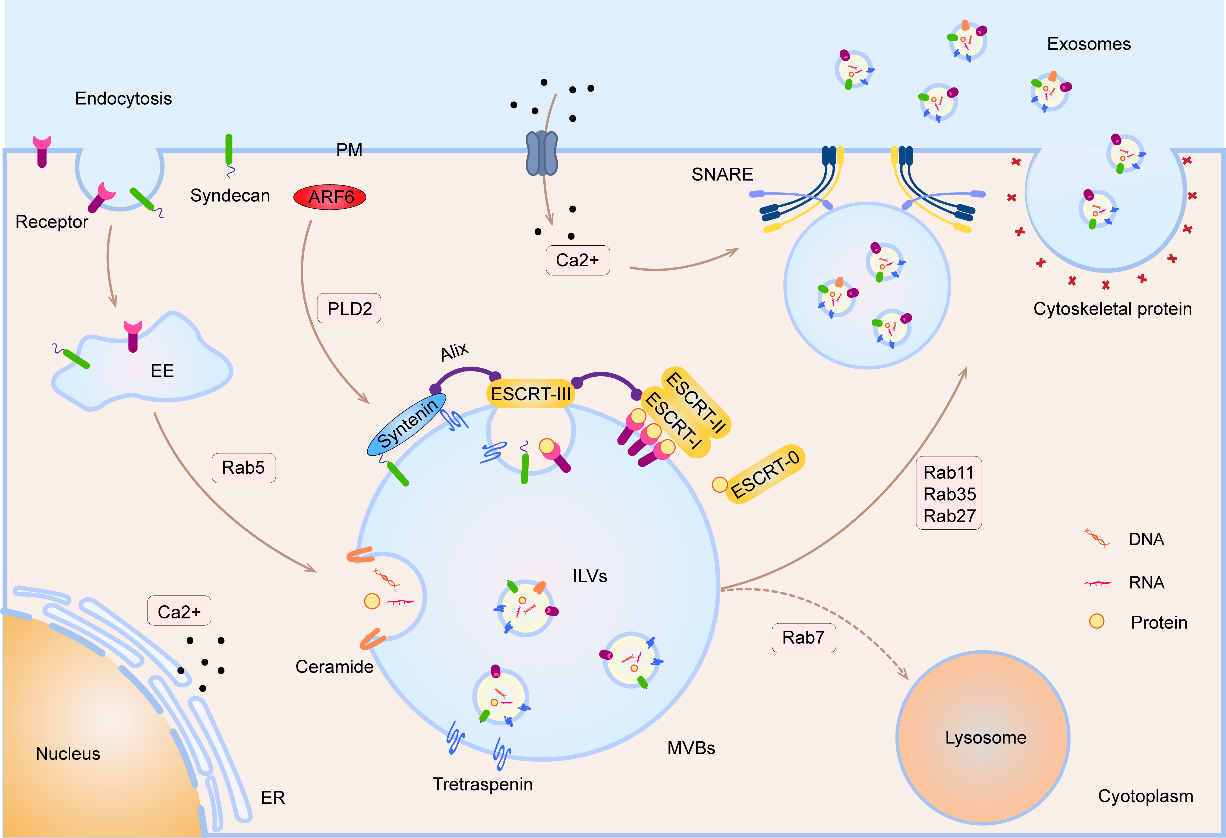
该综述首先介绍了外泌体的生成的机制,包括ESCRT依赖途径和非ESCRT依赖途径,并总结了调控外泌体形成和分泌的关键分子及其主要作用。外泌体的形成和分泌是一个受到精细调控的复杂过程,揭示并利用其背后的机制有利于研究其在生理和疾病状态中的作用以及有利于我们找到合适的位点进行干预,从而促进外泌体的形成和分泌,收获更多的外泌体。
图1 外泌体的形成和分泌机制
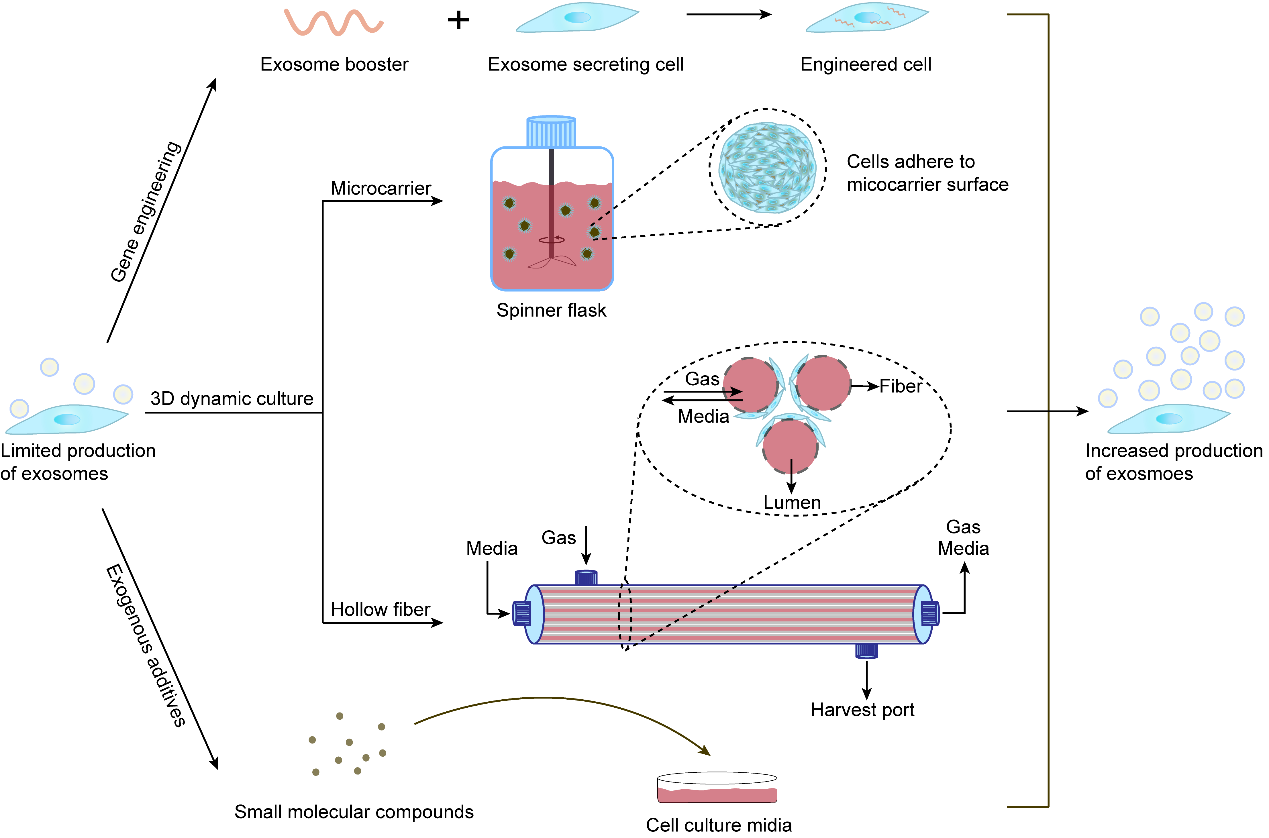
随后,文章主要从四个方面介绍了提高外泌体产量的方法:(1)通过基因工程改造细胞,调控外泌体形成和分泌过程中的关键分子促进外泌体分泌。(2)改变细胞培养条件,通过添加小分子化合物调节细胞能量代谢从而促进外泌体产生,或制造缺氧或饥饿等环境刺激细胞产生更多外泌体。(3)3D培养。大规模细胞培养是获得足够数量外泌体的基础。传统的2D细胞培养模式耗时费力,与之相比,3D培养模拟体内环境,更有利于细胞之间相互交流,并提供更多的扩增空间,在该微环境中培养的细胞表现出更高的活力及更强的外泌体分泌能力。目前多种生物反应器可用于3D培养,例如基于微载体的旋转生物反应器和中空纤维生物反应器。(4)优化外泌体分离纯化方法。分离外泌体常用的方法包括差速超速离心(UC)、密度梯度离心、切向流过滤(TFF)、尺寸排阻色谱(SEC)、基于聚合物的沉淀法和免疫磁珠捕获等,各有其优点和不足之处。目前UC仍是使用最广泛的方法,TFF是大规模分离外泌体最快的方法之一。新兴技术和新材料包括磁性纳米线、微流体和声流体等已被开发应用于外泌体的分离和纯化。
图2 提高外泌体产量的方法
最后,该综述概述了间充质干细胞来源外泌体在中枢神经系统疾病、心血管系统疾病和伤口愈合等的应用,介绍了间充质干细胞来源外泌体相关的临床试验及其剂量,并进一步讨论了外泌体临床转化中面临的挑战,包括批次间差异难以控制以及目前缺乏有效统一的标准规范外泌体产品等。外泌体从实验室走向临床,还有很多工作要做。
参考文献:
Challenges and strategies: Scalable and efficient production of mesenchymal stem cells-derived exosomes for cell-free therapy, Life Sci. 2023 Feb 22;319:121524. doi: 10.1016/j.lfs.2023.121524.
外泌体资讯网 【综述】Life Sciences|山东大学药学院王凤山、张新科团队:规模化生产间充质干细胞来源外泌体面临的挑战及相应的策略