脑胶质瘤是一类原发性程度较高的颅内恶性肿瘤,平均每10万人中就有5~8人患病;而五年病死率仅次于胰腺癌和肺癌,位列癌症死亡原因第三。由于脑胶质瘤细胞浸润性生长的特点,手术切除后通常需要辅助以化学药物治疗。尽管有一些新的治疗药物研发和上市,但是由于肿瘤的异质性和进展性,传统药物治疗在未来很长的时间仍然是肿瘤治疗的基石。但现有抗肿瘤药物的组织特异性差,毒副作用高;另外,血脑屏障的存在又可以阻挡超98%的小分子药物和几乎100%的大分子药物。因此,迫切需要开发瘤特异性和组织器官特异性的靶向递送药物载体。希望能够提高靶组织器官和肿瘤部位的药物浓度,实现增效减毒作用。通俗的讲就是需要一个特殊的包裹快递,而收件人的信息则是中枢神经系统的脑胶质瘤细胞。
外泌体是一类活细胞产生的纳米级细胞外囊泡,尺寸只有30~150 nm,具有典型的双层生物膜结构,并富含来自细胞的蛋白质、核酸和脂质等生物活性成分。在机体微环境中,外泌体从亲本细胞释放后被受体细胞摄取,在细胞与细胞间物质运输和信息传递中发挥重要作用,是一类天然的药物载体。借助于其纳米级尺寸和双层生物膜结构,外泌体具有穿越血脑屏障的天然属性。然而,将外泌体通过静脉移植后,绝大部分都会被肺、肝、脾等内脏器官摄取。
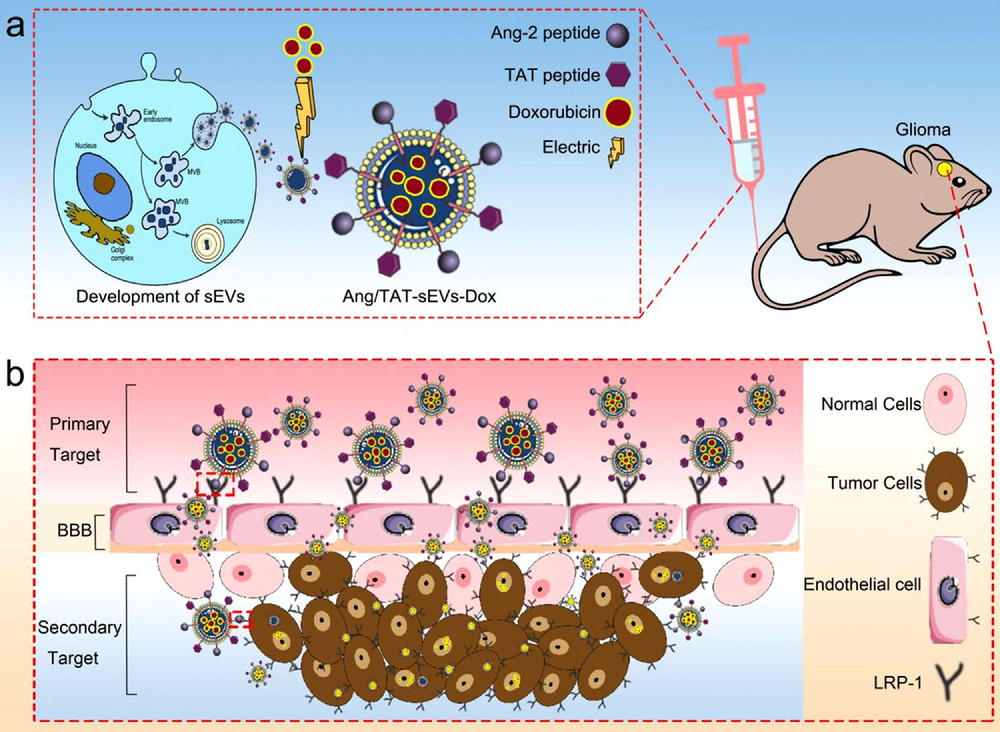
近日,中国科学院苏州纳米技术与纳米仿生研究所程国胜研究团队设计开发了Angiopep-2和TAT双重靶向功能化外泌体应用于脑胶质瘤的治疗研究。其中Angiopep-2多肽可以特异靶向低密度脂蛋白受体(LRP-1), LRP-1同时表达在脑胶质瘤细胞和脑血管内皮细胞表面;而跨膜多肽TAT可以提高外泌体对血脑屏障的穿透性。因此,通过静脉移植后,双重靶向功能化外泌体首先可以在血脑屏障表面富集,进而有效跨越血脑屏障,又可以被脑胶质瘤细胞摄取,进而提高了治疗药物的局部浓度。相关成果以“Specific anti-glioma targeted-delivery strategy of engineered small extracellular vesicles dual-functionalised by Angiopep-2 and TAT peptides”为题,于8月8日在国际细胞外囊泡杂志J Extracell Vesicles发表(2022 Aug;11(8):e12255)。文章第一作者为中国科学技术大学朱展翅博士,共同通讯作者为苏州九龙医院马三立博士和中科院苏州纳米所杨令延博士(现广州国家实验室副研究员)。相关研究得到广东省基础与应用基础研究基金联合基金重点项目(2019B1515120090)、国家自然科学基金青年基金项目(51903246,31700831)以及江苏省重点研发计(BK20201196)支持。
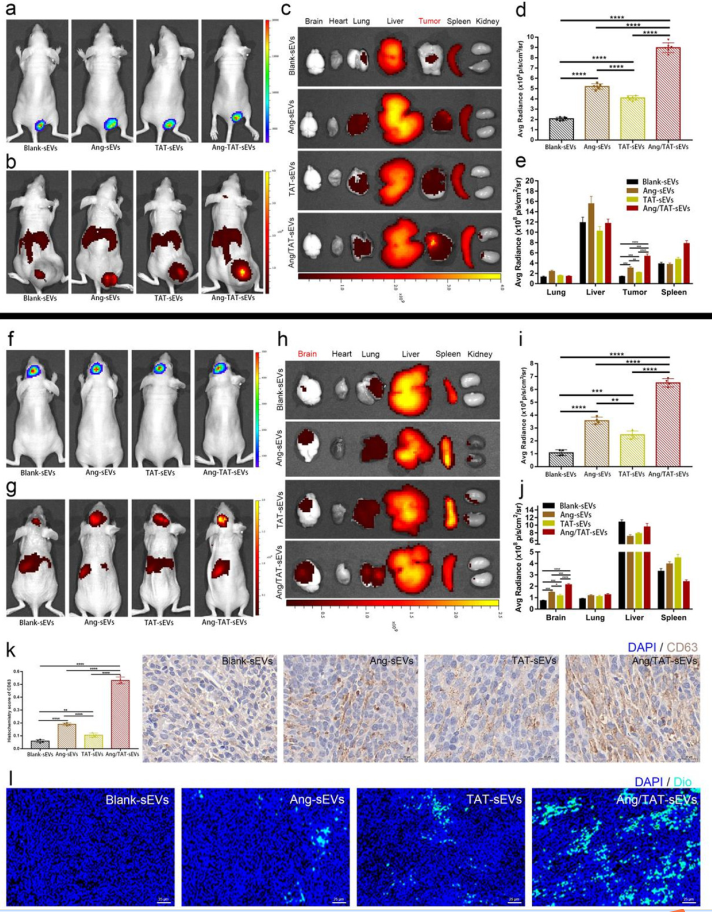
利用多种分子生物学和形态学技术评估发现,双重靶向功能化外泌体高效富集了靶向多肽,具有典型的双层生物膜和纳米级尺寸分布,没有受到工程化改造的影响。研究团队分别利用体外单细胞培养和Trans-well构建的体外血脑屏障模型,以及体内小鼠皮下脑胶质瘤模型和脑胶质瘤原位模型证实工程化外泌体对脑胶质瘤具有优良的靶向性。
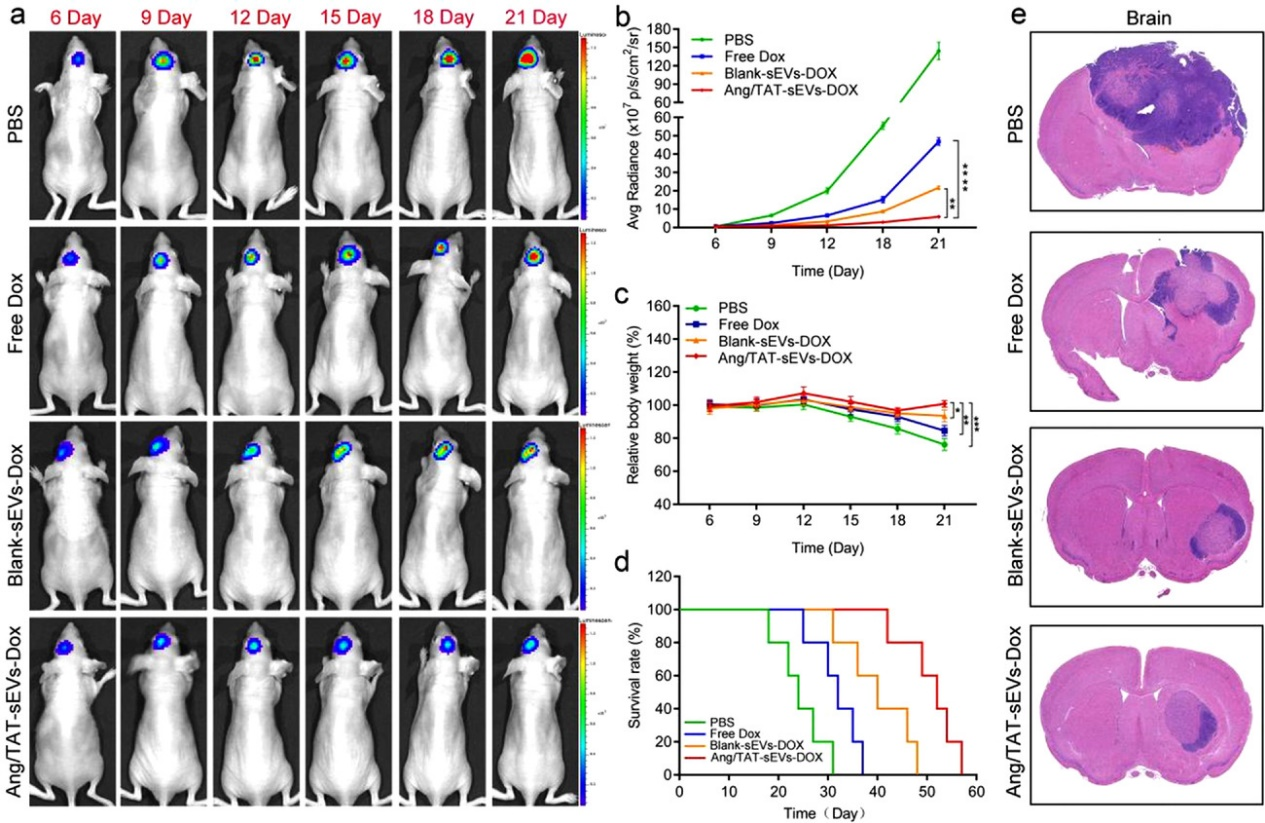
研究结果发现,双重靶向功能化外泌体能够提高药物治疗原位脑胶质瘤效率,有效改善小鼠生存期。同时,双重靶向功能化外泌体可以有效降低药物治疗毒副作用。
参考文献:Specific anti-glioma targeted-delivery strategy of engineered small extracellular vesicles dual-functionalised by Angiopep-2 and TAT peptides. J Extracell Vesicles. 2022 Aug;11(8):e12255. doi: 10.1002/jev2.12255.
外泌体资讯网 JEV | 中国科学院苏州纳米技术与纳米仿生研究所程国胜:Angiopep-2和TAT双重靶向功能化外泌体治疗脑胶质瘤的探索研究