DNAdamage-regulated autophagy modulator 1(DRAM1)是一种跨膜蛋白,有研究提示DRAM1能够在炎症、脂质积累以及细胞凋亡中发挥作用,然而其在以肝脏炎症和细胞凋亡为特征的酒精相关性肝病(Alcohol-related liver disease, ALD)中的作用仍不明确。ALD引发的炎症主要由巨噬细胞介导,M1型巨噬细胞可以释放促炎细胞因子并发挥促炎作用。目前针对ALD仍缺乏有效的治疗方法,急需探寻新的ALD诊疗靶点。
近日,青岛市市立医院辛永宁/庄立琨课题组在Mol Ther Nucleic Acids杂志上发表了题为“DRAM1increases the secretion of PKM2-enriched EVs from hepatocytes to promotemacrophage activation and disease progression in ALD”的文章,报道了DRAM1通过影响肝细胞分泌的细胞外囊泡(EVs)内容物进而激活巨噬细胞并加剧ALD的疾病进程,为探寻新的ALD诊断标志物和治疗靶点奠定理论基础。
首先,研究者在酒精诱导的早期阶段观察到了小鼠肝组织和肝细胞中DRAM1表达水平的明显升高。为了进一步探究DRAM1在ALD中的作用,研究者使用DRAM1基因敲除小鼠和DRAM1肝脏特异性过表达小鼠进行ALD模型的构建,发现DRAM1敲除可以明显减轻ALD小鼠的肝脏脂质积累和肝损伤程度,而DRAM1肝脏特异性过表达可显著加重小鼠ALD的疾病进程。
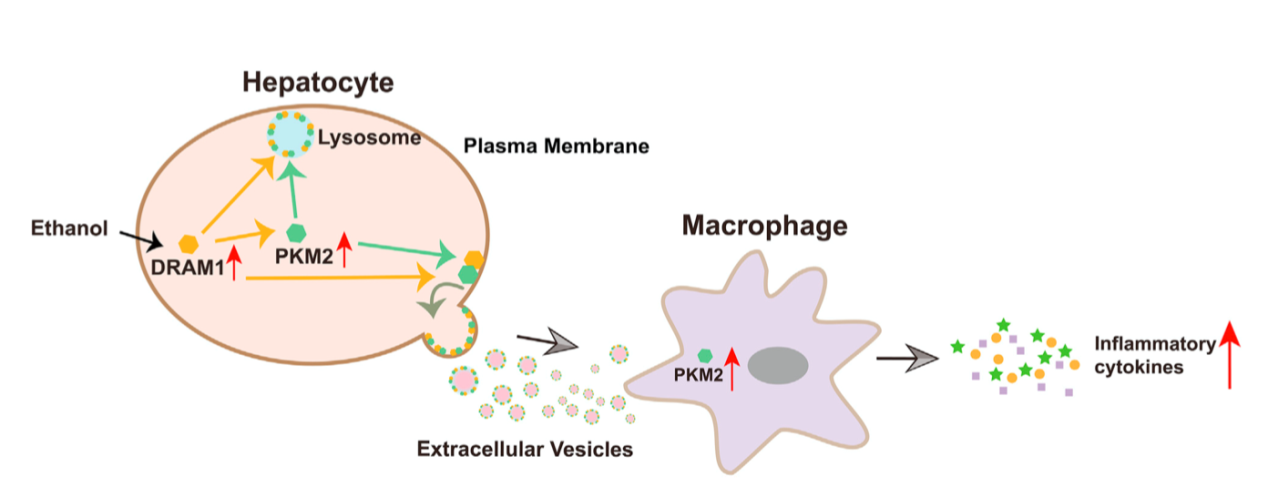
那么肝细胞中DRAM1如何影响ALD的发生发展?进一步实验结果表明,DRAM1过表达的肝细胞所释放的EVs能够促进巨噬细胞的活化和促炎细胞因子的表达;同时研究者在细胞和动物水平上均发现酒精诱导过程中肝细胞DRAM1介导了富含PKM2蛋白的EVs的释放,而PKM2能够诱导巨噬细胞的分化和活化。机制方面,研究者使用免疫共沉淀(co-IP)及免疫荧光实验证实了肝细胞中DRAM1能够与PKM2相互结合,DRAM1的过表达还能够增加PKM2蛋白的细胞膜定位。
最后,研究者探索了DRAM1在ALD患者肝组织中的表达水平。通过分析GEO数据库中包含ALD患者肝组织基因表达谱的数据集,研究者发现ALD患者肝组织中DRAM1表达水平和对照组相比显著上调,并且与M1型巨噬细胞标志物的表达水平呈明显正相关性。
本研究揭示了DRAM1介导的肝细胞和巨噬细胞之间的细胞通讯在ALD发生发展过程中发挥了重要的作用,同时提示DRAM1有潜力成为治疗ALD的有效靶标。
DRAM1在酒精处理肝细胞过程中的表达和作用机制图
参考文献:
DRAM1 increases the secretionof PKM2-enriched EVs from hepatocytes to promote macrophage activation anddisease progression in ALD. Mol Ther Nucleic Acids. 2021,11;27:375-389.
外泌体资讯网 Mol Ther Nucleic Acids|青岛市市立医院辛永宁/庄立琨组: 揭示细胞外囊泡加剧酒精性肝病进程的新机制