近日,华中科技大学生命科学与技术学院郭安源教授和华中科技大学同济医学院附属协和医院的胡豫教授和李秋柏教授在ScienceTranslational Medicine杂志(影响因子16.304)上发表文章,报道了新生儿脐带MSCs(UC-MSCs)来源的细胞外囊泡(UC-EVs)可以逆转成人骨髓MSCs(AB-MSCs)的衰老,显著增强后者成骨和损伤修复能力;特别是,体内应用UC-EVs可显著延缓自然衰老小鼠的衰老,对骨骼、肾脏以及血管平滑肌等多种组织器官的退行性变有显著影响。
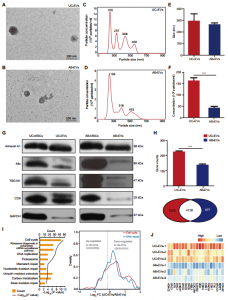
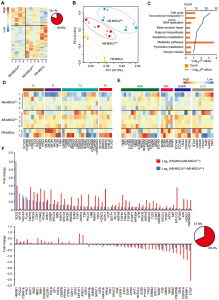
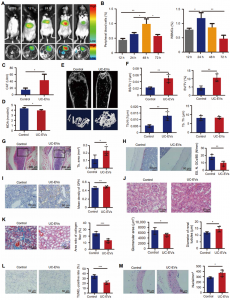
衰老与细胞、组织和机体水平的进行性功能衰退有关。以前在老年小鼠中进行的研究表明,用幼鼠的血液进行治疗可以减缓各个器官(包括脊髓、大脑、心脏和肌肉)中与年龄相关的变性过程。年轻人血液中存在的天然抗衰老因子仍然知之甚少,但这是一个非常活跃的研究领域,目前人们正在研究多种再生疗法。细胞衰老可以定义为与“定型”表型变化相关的细胞周期的稳定停滞,并且在许多组织中干细胞功能随着年龄的增长而下降。年轻的血液可以改善衰老小鼠各种干细胞的功能。间充质干细胞(MSCs)驻留在几乎所有哺乳动物器官的基质中,在组织再生过程中发挥重要作用,并能够分化为多种细胞谱系。例如,骨髓MSC(BMSC)分化为成骨细胞和脂肪细胞。BMSC被认为是用于再生细胞疗法的最有希望的种子细胞类型之一。然而,BMSC的体内衰老与器官变性和相关疾病(如骨质疏松症)的发展有关,与从胎儿组织分离的MSC相比,成年组织衍生的MSC的细胞增殖、干性和分化活性降低。具体而言,众所周知,衰老会影响成脂谱系和成骨谱系之间的平衡,并且已在尝试逆转或阻止MSC衰老。细胞外囊泡(EVs)是膜封闭的结构,主要分为两组。外泌体的直径范围为40至150 nm,来自内体系统;微囊泡的直径范围为100至1000 nm,是通过从质膜脱落而产生的。EVs通过将mRNA、微小RNA、蛋白质和细胞器货物转移到受体细胞中来促进细胞间通讯,并被认为是组织再生和修复的优秀候选治疗药物。最近发现,EVs似乎是延长小鼠寿命的年轻血液的有益成分,并且已假设循环EVs可介导年轻个体对抗衰老的有益作用。该研究发现,与成人BMSC衍生的EV(AB-EV)相比,新生的人类脐带(UC)MSC衍生的EV(UC-EV)包含更多的抗衰老信号。用UC-EV治疗衰老的成年骨髓MSC(AB-MSC)可以使这些细胞在生理和遗传水平上恢复活力。然后发现,UC-EVs将增殖细胞核抗原(PCNA)的mRNA转录物转移到受体AB-MSC中,这是AB-MSC再生过程所必需的。用这些再生的AB-MSC治疗的小鼠模型显示出积极的作用,将UC-EV静脉注射到衰老的小鼠中具有有希望的抗衰老特性。这项研究表明UC-EV含有抗衰老信号,可将衰老的AB-MSC成功地恢复为具有治疗活性的干细胞,并在小鼠中赋予抗衰老作用。脐带MSC-EVs(UC-EV)处理的成人骨髓MSC(AB-MSC)表现出胎儿骨髓(FB-MSC)的基因表达模式总之,该研究证明了新生儿脐带(UC)是间充质干细胞的EV(MSC-EV)的来源。这些由UC产生的MSC-EV(UC-EV)包含丰富的抗衰老信号,并能使衰老的成年骨髓衍生MSC(AB-MSC)恢复活力。UC-EV处理的AB-MSCs表现出缓解的衰老表型,并增加了自我更新能力和端粒长度。从机理上讲,UC-EV通过将增殖细胞核抗原(PCNA)转移到受体AB-MSC中来至少部分使AB-MSC再生。在治疗环境中进行测试时,UC-EV触发的年轻化增强了AB-MSC在骨骼形成、伤口愈合和血管生成中的再生能力。静脉注射的UC-EV赋予抗衰老表型,包括减少老年小鼠的骨骼和肾脏变性。该发现表明,UC-EV在抗衰老干预中具有很高的转化价值。UC-EV的静脉治疗可缓解多种与年龄相关的小鼠表型Lei,Q., et al. (2021). "Extracellular vesicles deposit PCNA to rejuvenateaged bone marrow-derived mesenchymal stem cells and slow age-relateddegeneration." Science Translational Medicine13(578).外泌体资讯网 Science子刊:新生儿脐带MSCs来源的EVs可逆转衰老