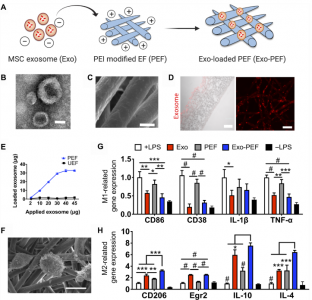
近日,北京大学罗莹教授课题组在Science Advances杂志上发表文章,报道了间充质基质细胞(MSC)外泌体功能化的纤维状聚酯材料支架,通过诱导先天和适应性免疫反应,促进组织损伤的修复。
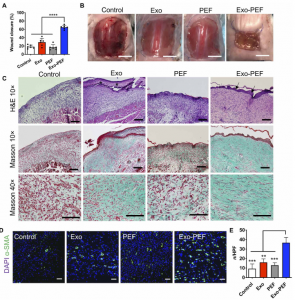
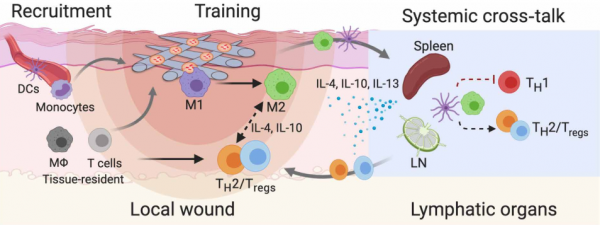
 免疫系统不仅是人体抵御病原体入侵的第一道防线,而且在介导组织发育、体内平衡和修复过程中也起着关键作用。通过各种精细的事件,免疫细胞和介体通过参与炎症、血管生成和干/祖细胞活性(例如增殖和分化)来影响组织的修复和再生过程。在先天免疫反应中,发现从促炎性M1样向修复性M2样表型的巨噬细胞(MΦ)极化足以促进组织修复。适应性免疫细胞在与先天细胞的双向通讯中也很活跃:CD4+ T辅助2(TH2)细胞和调节性T细胞(Tregs)能够分泌细胞因子,例如白介素4(IL-4)和IL-10和转化生长因子-β(TGF-β)以促进MΦ向免疫调节性M2样表型的转变。Tregs还产生可直接诱导组织驻留祖细胞/干细胞增殖和分化的生长因子。另一方面,CD8+ T细胞和CD4+ TH1细胞分泌肿瘤坏死因子-α(TNF-α)和干扰素-γ(IFN-γ),这将延长促炎性MΦ的存在并诱导干细胞凋亡。设计生物材料以调节免疫系统朝着再生应答的方向,可以为再生医学的未来发展指明方向。近年来开始对生物材料范围内的先天性和适应性免疫反应进行研究,表明生物功能支架可以通过调节局部MΦ及其与T细胞的串扰来促进组织再生。然而,了解和设计支架材料和生物制剂在引发有益免疫反应方面的作用,尤其是在全身水平上,尚待探索。为此,通过将来源于间充质基质细胞(MSCs)的外泌体固定在纤维状聚合物网上,构建了一种新型的无细胞生物支架,研究了皮肤伤口模型中局部组织以及远端淋巴器官的先天性和适应性免疫反应。从细胞释放的外泌体,以膜包围的细胞外囊泡的形式,传递蛋白质和核酸,以介导细胞间的通讯。特别地,已知从各种组织中收获的MSC具有免疫调节功能,并在移植手术和移植物抗宿主疾病的治疗中提供了有希望的治疗选择。与MSC相似,MSC外泌体相关的免疫调节功能涉及促进M2样MΦ表型、Treg群体和TH2免疫反应。作为活细胞的替代品,MSC外泌体有望用作生物实体,以开发具有等效或更高疗效的疗法。该研究旨在了解支架和外泌体是否可以开发为组合的无细胞系统,以启动局部和全身水平的协同免疫反应。这项研究可能潜在地促进新的生物功能支架的开发,基于这些系统在宿主中复杂的生物环境中的作用机制。MSC外泌体功能化的纤维支架对体外培养的巨噬细胞具有免疫调节作用设计能够诱导和指导适当的免疫反应的支架为组织修复/再生提供了希望。该研究通过将间充质基质外泌体固定在纤维状聚酯材料(Exo-PEF)上,并允许细胞介导的膜结合囊泡的递送来制备生物功能支架。定量的细胞水平分析显示,免疫细胞在体内从支架中摄取外泌体占主导地位,材料和外泌体分别充当免疫细胞的募集者和训练者,以协同促进小鼠皮肤伤口中有益的巨噬细胞和调节性T细胞反应。发现适应性T辅助细胞反应在远端免疫器官中活跃,并且在大型皮肤损伤模型中,载有外泌体的支架促进了组织修复。这项研究证明了对生物植入物的局部和全身免疫反应涉及的重要机制,并且对组织修复性免疫调节的了解可能指导新型生物功能支架的设计。Exo-PEF在2周内治愈了大的皮肤伤口,显示出伤口闭合、上皮再形成、胶原蛋白沉积和血管形成模式图:Exo-PEF材料促进组织修复中涉及的免疫调节机制可能包括(i)募集和训练免疫细胞,(ii)抗炎介质的作用,以及(iii)远程免疫器官的作用SuN, Hao Y, Wang F, Hou W, Chen H, Luo Y. Mesenchymal stromal exosome-functionalized scaffolds induce innate and adaptive immunomodulatory responses toward tissue repair. Science Advances. 2021May 12;7(20):eabf7207. PMID: 33980490.
免疫系统不仅是人体抵御病原体入侵的第一道防线,而且在介导组织发育、体内平衡和修复过程中也起着关键作用。通过各种精细的事件,免疫细胞和介体通过参与炎症、血管生成和干/祖细胞活性(例如增殖和分化)来影响组织的修复和再生过程。在先天免疫反应中,发现从促炎性M1样向修复性M2样表型的巨噬细胞(MΦ)极化足以促进组织修复。适应性免疫细胞在与先天细胞的双向通讯中也很活跃:CD4+ T辅助2(TH2)细胞和调节性T细胞(Tregs)能够分泌细胞因子,例如白介素4(IL-4)和IL-10和转化生长因子-β(TGF-β)以促进MΦ向免疫调节性M2样表型的转变。Tregs还产生可直接诱导组织驻留祖细胞/干细胞增殖和分化的生长因子。另一方面,CD8+ T细胞和CD4+ TH1细胞分泌肿瘤坏死因子-α(TNF-α)和干扰素-γ(IFN-γ),这将延长促炎性MΦ的存在并诱导干细胞凋亡。设计生物材料以调节免疫系统朝着再生应答的方向,可以为再生医学的未来发展指明方向。近年来开始对生物材料范围内的先天性和适应性免疫反应进行研究,表明生物功能支架可以通过调节局部MΦ及其与T细胞的串扰来促进组织再生。然而,了解和设计支架材料和生物制剂在引发有益免疫反应方面的作用,尤其是在全身水平上,尚待探索。为此,通过将来源于间充质基质细胞(MSCs)的外泌体固定在纤维状聚合物网上,构建了一种新型的无细胞生物支架,研究了皮肤伤口模型中局部组织以及远端淋巴器官的先天性和适应性免疫反应。从细胞释放的外泌体,以膜包围的细胞外囊泡的形式,传递蛋白质和核酸,以介导细胞间的通讯。特别地,已知从各种组织中收获的MSC具有免疫调节功能,并在移植手术和移植物抗宿主疾病的治疗中提供了有希望的治疗选择。与MSC相似,MSC外泌体相关的免疫调节功能涉及促进M2样MΦ表型、Treg群体和TH2免疫反应。作为活细胞的替代品,MSC外泌体有望用作生物实体,以开发具有等效或更高疗效的疗法。该研究旨在了解支架和外泌体是否可以开发为组合的无细胞系统,以启动局部和全身水平的协同免疫反应。这项研究可能潜在地促进新的生物功能支架的开发,基于这些系统在宿主中复杂的生物环境中的作用机制。MSC外泌体功能化的纤维支架对体外培养的巨噬细胞具有免疫调节作用设计能够诱导和指导适当的免疫反应的支架为组织修复/再生提供了希望。该研究通过将间充质基质外泌体固定在纤维状聚酯材料(Exo-PEF)上,并允许细胞介导的膜结合囊泡的递送来制备生物功能支架。定量的细胞水平分析显示,免疫细胞在体内从支架中摄取外泌体占主导地位,材料和外泌体分别充当免疫细胞的募集者和训练者,以协同促进小鼠皮肤伤口中有益的巨噬细胞和调节性T细胞反应。发现适应性T辅助细胞反应在远端免疫器官中活跃,并且在大型皮肤损伤模型中,载有外泌体的支架促进了组织修复。这项研究证明了对生物植入物的局部和全身免疫反应涉及的重要机制,并且对组织修复性免疫调节的了解可能指导新型生物功能支架的设计。Exo-PEF在2周内治愈了大的皮肤伤口,显示出伤口闭合、上皮再形成、胶原蛋白沉积和血管形成模式图:Exo-PEF材料促进组织修复中涉及的免疫调节机制可能包括(i)募集和训练免疫细胞,(ii)抗炎介质的作用,以及(iii)远程免疫器官的作用SuN, Hao Y, Wang F, Hou W, Chen H, Luo Y. Mesenchymal stromal exosome-functionalized scaffolds induce innate and adaptive immunomodulatory responses toward tissue repair. Science Advances. 2021May 12;7(20):eabf7207. PMID: 33980490.外泌体资讯网 北京大学罗莹教授:间充质干细胞外泌体功能化的材料支架促进组织修复 | Science Advances