间充质干细胞来源的外泌体microRNA是一种有前景的癌症治疗策略。来自郑州大学第一附属医院赵松教授课题组的研究人员在Journal of Experimental and Clinical Cancer Research杂志上发表文章,阐明了人脐带间充质干细胞衍生的外泌体miR-375通过抑制ENAH的表达而抑制食管鳞状细胞癌发展的机制。
食道癌是最普遍和最具侵略性的癌症类型之一,在全球癌症相关死亡中排名第六,并且在中国的年发病率特别高。食道癌被广泛认为具有两种临床亚型,食道腺癌和食道鳞状细胞癌(ESCC)。ESCC由于其预后特别差,所以是一种更危险的食道癌亚型,这很大程度上归因于其诊断时即晚期。尽管在诊断、手术技术和术后护理等方面已取得了可喜的进步,但ESCC患者的复发可能性还是很大。
间充质干细胞(MSCs)是肿瘤微环境的关键组成部分,并且MSCs衍生的β-2-微球蛋白参与ESCC的上皮间充质转化、迁移和肿瘤生长过程。人脐带间充质干细胞(hUCMSCs)可以在各种生物学过程中分泌外泌体,而hUCMSCs衍生的外泌体(hUCMSCs-exos)已成为潜在的疾病治疗剂。
作为各种细胞类型分泌的细胞外囊泡,外泌体可作为非侵入性生物标记物,用于早期诊断各种类型的癌症,并有望作为治疗剂。hUCMSCs-exo可以减轻炎症并促进脊髓损伤小鼠的功能恢复。更重要的是,hUCMSCs-exo通过递送外源性装载的miR-145-5p,抑制胰腺导管腺癌的进展。
包括miR-375在内的众多microRNA(miRNA或miRs)已被认为是ESCC患者的有希望的诊断和预后生物标志物。miR-375的表达下调在ESCC中很常见,并预示着预后差、存活率低和肿瘤转移。此外,细胞分泌的外泌体可能将治疗性miRNA传递给癌细胞和邻近细胞。外泌体miRNAs在包括癌症在内的各种人类疾病的发展中发挥作用。例如,外泌体miR-21可作为实验性ESCC治疗的有希望的靶标。
在这项研究中,研究人员通过生物信息学数据库,预测miR-375靶向enabled homolog蛋白(ENAH)。ENAH通常被称为Mena,是Ena /血管扩张剂刺激的磷蛋白家族的成员,由与肌动蛋白相关的蛋白组成,ENAH在各种细胞中发挥不同的作用。此外,ENAH在胃癌中高表达,并明显促进其发展,具有作为胃癌患者预后标志物的潜力。基于文献探索,研究人员猜想,外泌体miR-375通过调节ENAH表达有助于ESCC的发展。
在确定miR-375在ESCC组织和细胞中调节ENAH的表达后,研究人员检测了该机制对ESCC增殖、侵袭、迁移和肿瘤微球形成的影响。研究人员分离转染后的hUCMSCs来源的外泌体(hUCMSCs-exo),并与ESCC细胞共培养,检测hUCMSCs-exo递送的miR-375对ESCC发展的影响。同时,研究人员验证了miR-375对体内肿瘤生长的影响。结果显示,在ESCC中,miR-375的表达降低,而ENAH的表达升高。ENAH被确定为miR-375的靶基因。升高miR-375表达或降低ENAH表达均可以抑制ESCC细胞增殖、侵袭、迁移、肿瘤微球形成并促进凋亡。此外,由hUCMSCs-exo递送的miR-375可以抑制ESCC细胞增殖、侵袭、迁移、肿瘤微球形成,在体外促进细胞凋亡,并在体内抑制肿瘤生长。通过这些体外和体内实验,研究人员确定了hUCMSCs-exo传递的miR-375在ESCC发展中的潜在机制。
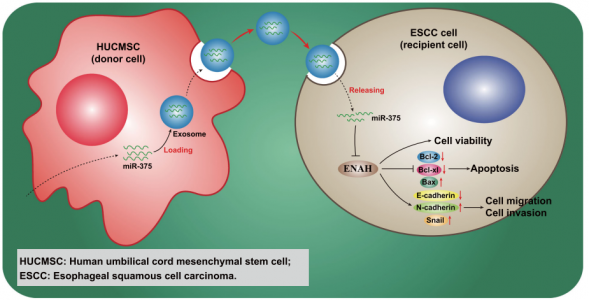
图:示意图显示了外泌体miR-375调控ESCC进程的分子机制。miR-375通过hUCMSCs-exo传递到ESCC细胞中,降低ENAH的表达,并随后增加Bax和E-cadherin的表达,并减少N-cadherin、Snail、Bcl-2和Bcl-xl的表达,从而减少ESCC细胞的增殖、侵袭和迁移并增强细胞凋亡。