土豆
巨噬细胞的M1促炎表型是非酒精性脂肪肝疾病(NAFLD)进展中的重要过程,但潜在的分子机制仍然不完全清楚。来自上海交通大学医学院附属新华医院范建高课题组的研究人员发现,脂毒性损伤后的肝细胞衍生外泌体在肝细胞和巨噬细胞之间通信在NAFLD进展中起到促进作用,其机制是通过调节Rictor/Akt/FoxO1信号传导以及M1巨噬细胞活化实现的。该研究发表于Hepatology杂志上。
非酒精性脂肪肝疾病(NAFLD)是影响全球约四分之一人口的最常见的全球健康问题,该疾病包括非酒精性脂肪肝(NAFL)、非酒精性脂肪性肝炎(NASH)以及相关的肝纤维化和肝硬化。NASH定义是存在严重的肝脂肪变性和肝细胞损伤的炎症。肝细胞损伤既是肝炎症的主要原因,也是继发的后果,因为受损的肝细胞会诱导巨噬细胞和其他免疫细胞的浸润和活化,从而依次释放各种炎症介质和细胞因子。炎性M1巨噬细胞极化的诱导和Kupffer细胞的活化在NAFLD的发展中起着关键作用。但是,尚不完全了解巨噬细胞识别肝细胞损伤信号的潜在分子机制以及控制巨噬细胞极化和激活的因素。
细胞外的miRNA在不同肝脏疾病中的细胞间通讯中非常重要。细胞外miRNA通过不同的过程从细胞中分泌出来,例如封装在细胞外小泡(如外泌体)中、与蛋白(如Ago2)结合以及一些其他机制。大多数细胞外miRs是通过外泌体分泌的,特别是当细胞损伤不严重时。外泌体是调节各种生理和病理生理过程的重要因素,在从NAFL到NASH的发展过程中起到了重要作用。据报道,miRNA通过与靶mRNA的3'非翻译区(UTR)中的部分互补位置配对,通过靶基因的转录后沉默来调节NAFLD中的脂质代谢、炎症和纤维化。miR-192-5p是肝脏组织中最丰富的miRNA之一,研究表明血清miR-192-5p水平可用作NAFLD疾病进展的潜在生物标志物。尽管外泌体已被确定为不同类型的细胞和器官之间相互影响的重要介质,但NAFLD/NASH中外泌体在肝细胞miR-192-5p介导的巨噬细胞活化调节中的作用仍有待探索。
Rictor是mTORC2的必不可少的亚基和主要效应物,其催化Akt Ser473位点的磷酸化。Akt介导的FoxO1的磷酸化导致FoxO1的核排出。 FoxO1的磷酸化和泛素化导致其降解。 FoxO1条件性基因敲除小鼠的先前研究显示,FoxO1在肝脏巨噬细胞极化中起重要作用。此外,Rictor是人类和啮齿动物中miR-192-5p的四个预测靶基因之一。因此,Rictor-Akt-FoxO1轴可能是miR-192-5p介导NAFLD中巨噬细胞激活和M1极化的关键信号通路。
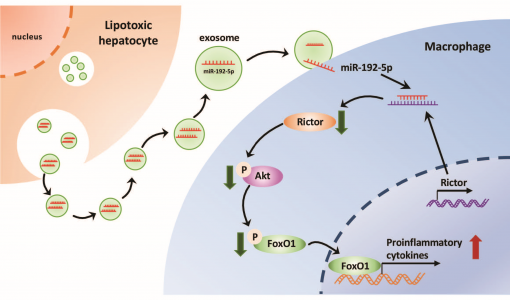
在本研究中,研究人员报道了脂毒性损伤诱导的富含miR-192-5p的肝细胞外泌体的释放在激活M1巨噬细胞和肝脏炎症中的关键作用。NAFLD患者的血清miR-192-5p水平与肝炎性活动评分和疾病进展呈正相关。同样,在高脂高胆固醇饮食(HFHCD)喂养的大鼠模型中,血清miR-192-5p水平、M1巨噬细胞数量、肝促炎介质的表达水平均与疾病进展相关。脂毒性肝细胞释放出比对照组更多的富含miR-192-5p的外泌体,从而诱导M1巨噬细胞(CD11b+ CD86+)活化并增加iNOS、IL-6和TNF-α的表达。此外,源自肝细胞的外泌体miR-192-5p抑制了Rictor的蛋白表达,从而进一步抑制了Akt和FoxO1的磷酸化水平,并导致FoxO1的激活和随后的炎症反应的诱导。
本研究揭示了肝细胞来源的外泌体miR-192-5p通过调节Rictor/Akt/FoxO1信号传导在促炎性巨噬细胞活化和NAFLD疾病进展中起关键作用。血清外泌体miR-192-5p可作为非酒精性脂肪性肝炎的潜在非侵入性生物标志物和治疗靶标。
参考文献:Liu XL, Pan Q, Cao HX, Xin FZ, Zhao ZH, Yang RX, Zeng J, Zhou H, Fan JG. Lipotoxic Hepatocyte-Derived Exosomal miR-192-5p Activates Macrophages via Rictor/Akt/FoxO1 Signaling in NAFLD. Hepatology. 2019 Nov 28. doi: 10.1002/hep.31050.