土豆
干细胞及其分泌的外泌体在促进骨再生方面具有相似的作用。研究表明,脐带间充质干细胞(uMSCs)可促进血管生成。近日,来自海军军医大学附属长海医院许硕贵、方硕课题组的研究人员在cell proliferation杂志发表论文,发现uMSC来源的外泌体可以通过促进血管生成来增强骨折愈合。该研究揭示了外泌体在uMSC介导的治疗中的新作用。
骨折愈合是一个复杂的过程,其中包括由一些生长因子和细胞因子调节局部间充质干细胞或祖细胞的活化、增殖和分化。大约5%-10%的骨折发生延迟愈合甚至不愈合,这两种情况都需要长期或重复治疗,对治疗成本和生活质量产生重大影响。
移植骨髓间充质干细胞(BMSCs)已被证明可增强骨生成和血管生成。然而,这些细胞的临床应用仍然受到来源有限、疼痛和创伤性以及安全性的阻碍。随着间充质干细胞在组织再生中的深入了解,越来越多的研究转向于间充质干细胞释放的外泌体(Exos)。已经证明这些40-100nm的细胞外囊泡在各种组织(神经、心肌、皮肤、骨骼肌及对应的干细胞等)的再生中具有相似的作用。外泌体被认为具有通过将某些蛋白质、遗传信息或其他分子转移至靶细胞来调节细胞活性的能力。此外,外泌体膜的特定脂质双层可以保护生物活性物质在不利条件下免于降解,并且外泌体稳定的物理和化学性质使它们易于在体外保存。因此,外泌体为研究人员提供了一种促进骨折愈合的新颖且有前景的方法。
脐带间充质干细胞(uMSC)具有易收集、增殖和分化能力强、免疫原性低的优点,已被证明通过增强血管生成在骨再生中是有效的。然而,关于骨再生的uMSC衍生的外泌体(uMSC-Exos)的研究很少有报道。研究人员认为,外泌体的治疗效果可能与其亲本干细胞类似,因此使用uMSC作为细胞来源来产生外泌体并研究这些外泌体是否可以通过促进血管生成或以其他方式增强骨折愈合。
在本研究中,研究人员利用uMSC,并通过超速离心分离uMSC-Exos,其中来自人胚肾293细胞(HEK293)外泌体和PBS用作对照组。 NanoSight、激光散射光谱仪、透射电子显微镜和蛋白质印迹用于鉴定外泌体。然后将uMSC-Exos与水凝胶结合移植到股骨骨折大鼠模型的骨折部位。在手术后第7、14、21和31天通过放射学方法监测和评估骨愈合过程;在术后第14天通过放射学和组织学方法评估骨折部位的血管生成。在体外,通过qRT-PCR鉴定与uMSC-Exos共培养后的成骨或血管生成相关基因的表达水平。使用PKH67测定确定外泌体的吸收能力。通过细胞周期分析、EdU实验和免疫荧光染色、划痕实验和微管形成分析,研究者确定uMSC-Exos处理的人脐静脉内皮细胞(HUVEC)在增殖、迁移和血管生成中的改变。在分子机制上,使用特异性RNA抑制剂或siRNA,并观察实验结果。
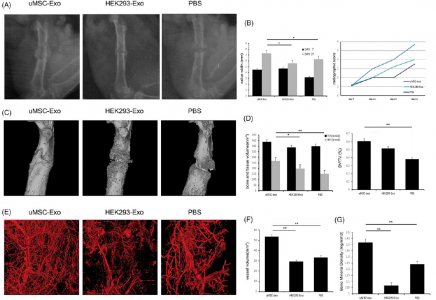
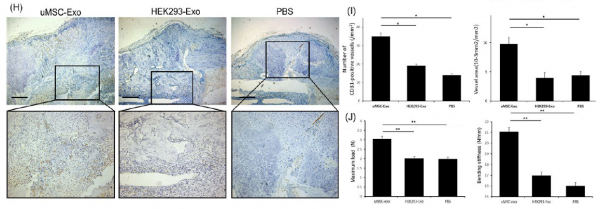
结果发现,研究人员将uMSC-Exos移植到股骨骨折大鼠模型的骨折部位后,观察到血管生成增强以及骨愈合过程加速。在体外,除了促进成骨分化外,uMSC-Exos增加血管内皮生长因子(VEGF)和缺氧诱导因子-1α(HIF-1α)的表达,促进人脐静脉内皮细胞(HUVECs)的增殖、迁移和微管形成。通过使用特异性RNA抑制剂或siRNA,研究人员证明uMSC-Exos可以通过调节HIF-1α改变内皮细胞的血管生成能力,这可能是促进骨折愈合的潜在机制之一。
图:uMSC-Exos移植到股骨骨折大鼠模型后,骨折愈合的放射学和组织学分析
参考文献:Zhang Y, Hao Z, Wang P, Xia Y, Wu J, Xia D, Fang S, Xu S. Exosomes from human umbilical cord mesenchymal stem cells enhance fracture healing through HIF-1α-mediated promotion of angiogenesis in a rat model of stabilized fracture. Cell Prolif. 2019 Jan 20:e12570.
外泌体资讯网 海军军医大学许硕贵、方硕课题组:人脐带间充质干细胞分泌的外泌体通过HIF-1α介导的血管生成促进大鼠骨折愈合