甲状腺癌是最常见的内分泌恶性肿瘤,其中约2%的甲状腺癌是甲状腺未分化癌(anaplastic thyroid carcinoma, ATC),是最致命和具治疗抗性的人类癌症之一。肿瘤干细胞样细胞(CSC)可以引发肿瘤发生,诱导对化学疗法和放射疗法的抗性,具有多种促肿瘤能力并且可能导致复发和转移。CSC的产生与上皮间质转化(EMT)和干性的获得有关。外泌体是由大多数细胞分泌的小(30-150nm)膜囊泡,其在细胞间通信中起重要作用。许多非编码RNA(ncRNA),例如长链非编码RNA(lncRNA),可以启动肿瘤发生和EMT过程,而外泌体可以携带ncRNA到局部和远端细胞。
本研究从两种体外培养的细胞(EMT模型细胞和CSC模型细胞)中检测分泌的外泌体。通过TGFβ-1处理在甲状腺乳头状癌(PTC)细胞系中诱导EMT。分离来自该细胞模型的外泌体并与初始PTC细胞共培养并检测EMT诱导情况。在CSC模型中,从CSC细胞系中分离外泌体,与正常甲状腺细胞系一起培养并检测EMT诱导。 EMT外泌体能够转移lncRNA MALAT1和EMT效应因子SLUG和SOX2。然而,在该模型中没有诱导EMT的发生。来自CSC模型的外泌体也转移了lncRNA MALAT1和转录因子SLUG和SOX2,但它们会另外转移linc-ROR并在正常甲状腺细胞中诱导了EMT。利用siRNA干扰linc-ROR的初步研究发现细胞侵袭减少。威斯康星大学医学与公共卫生学院的研究人员假设CSC外泌体转移lncRNAs,包括linc-ROR在内,诱导EMT并建立局部肿瘤微环境和远处转移生态位。靶向CSC及其分泌的外泌体和它们携带的lncRNA的疗法可以降低肿瘤的转移能力。
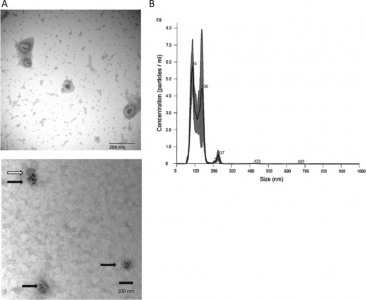
图:甲状腺癌细胞TPC-1的外泌体鉴定、CD9阳性的胶体金鉴定和粒子大小分布。
参考文献:Hardin H, Helein H, Meyer K, Robertson S, Zhang R, Zhong W, Lloyd RV. (2018) Thyroid cancer stem-like cell exosomes: regulation of EMT via transfer of lncRNAs. Lab Invest [Epub ahead of print].